Анион и катион — это два важных понятия в химии, которые описывают заряженные частицы в химических соединениях. Анион представляет собой отрицательно заряженный ион, который получает дополнительные электроны. Катион же — это положительно заряженный ион, который теряет электроны. Оба этих типа ионов играют важную роль в реакциях, так как их взаимодействие способствует образованию стабильных химических соединений.
Примеры анионов включают такие ионы, как хлорид(Cl-), сульфат(SO42-), нитрат(NO3-). Примеры катионов могут быть ионами металлов, такими как натрий(Na+), калий(K+), кальций(Ca2+).
Определение аниона

Давай разберемся, что это означает в более понятной форме. Все атомы стремятся достичь электронной конфигурации инертного газа, чтобы быть стабильными. Это означает, что они хотят заполнить свою внешнюю электронную оболочку полностью. А они могут это сделать, либо отдавая, либо получая электроны.
Когда атом или молекула получает один или несколько электронов от другого атома или молекулы, он становится отрицательно заряженным, потому что число электронов становится больше числа протонов. Это и есть анион.
Анионы имеют очень важную роль в химии. Они являются одним из двух основных типов ионов, второй тип называется катион. Катионы заряжены положительно, в отличие от анионов, которые заряжены отрицательно.
Анионы играют решающую роль во многих процессах, связанных с электролитами, реакциями окисления-восстановления, а также в составлении кристаллических структур и межмолекулярных связей. Они также служат для поддержания электрической нейтральности в химических соединениях.
Вот некоторые примеры анионов: гидроксидный ион (OH-), хлоридный ион (Cl-), нитратный ион (NO3-), сульфатный ион (SO4-2) и многие другие. Они встречаются в различных химических соединениях и имеют важные свойства и применения.
Итак, чтобы ответить на вопрос, что такое анион, мы можем сказать, что это негативно заряженная частица, которая образуется при получении электронов атомом или молекулой. Анионы играют ключевую роль в химии и имеют широкий спектр свойств и применений.
Определение катиона
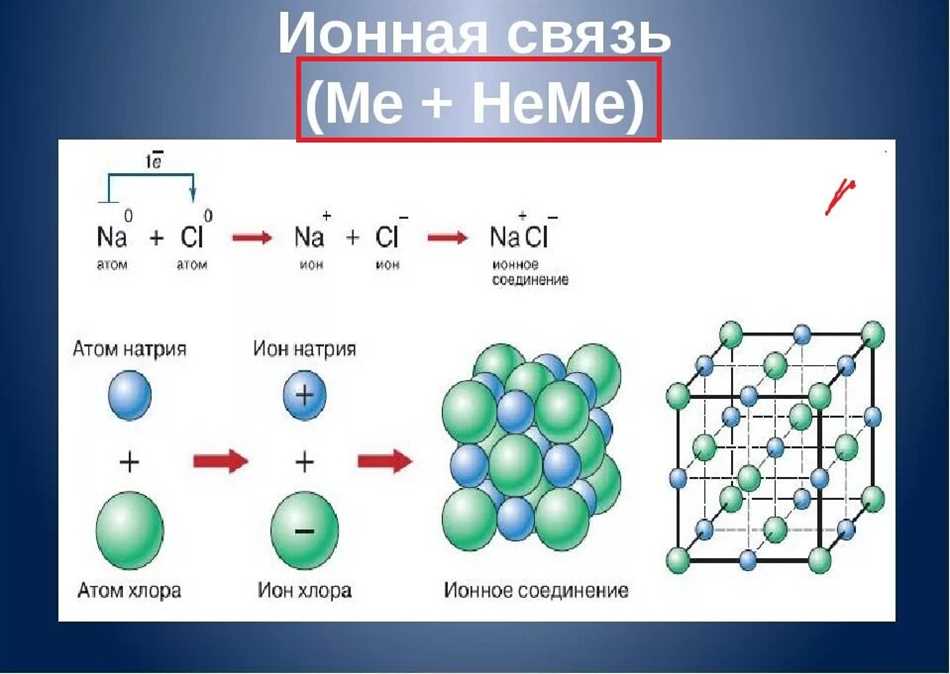
Катион – это положительно заряженная частица, которая образуется путем потери одного или нескольких электронов атомом или молекулой. У нас есть много примеров катионов, которые вы можете найти в повседневной жизни.
Давай я приведу тебе несколько примеров. Первый пример – ионы натрия. Натрий – это химический элемент, который мы часто встречаем в нашей пище. Когда атом натрия теряет один электрон, он становится положительно заряженным катионом. Возможно, ты слышал о таких веществах, как поваренная соль или еда из фастфуда, они содержат ионы натрия.
Еще один пример – ионы кальция. Кальций – это элемент, который играет важную роль в нашем организме, особенно для здоровья костей и зубов. Когда атом кальция теряет два электрона, он становится положительно заряженным катионом. Продукты, богатые кальцием, такие как молоко и йогурт, содержат ионы кальция.
Теперь, когда ты знаешь, что такое катион, давай посмотрим, зачем это нужно и как они влияют на нашу жизнь. Катионы играют важную роль во многих химических реакциях и процессах в организмах живых существ.
В биологии, ионы натрия и калия участвуют в передаче нервных импульсов в нашем организме. Это означает, что без ионов катионов мы не смогли бы передавать сигналы в наших нервах, что привело бы к серьезным нарушениям в функционировании нашего организма.
Катионы также являются неотъемлемой частью процессов взаимодействия веществ в химии. Ионы катионы могут быть использованы для стабилизации растворов, изменения pH-уровня веществ и даже для улучшения вкуса и запаха.
Различия между анионами и катионами
Пожалуй, самое заметное различие между анионами и катионами — это заряд, который они несут. Анионы имеют отрицательный заряд, в то время как катионы имеют положительный заряд. Это происходит из-за разницы в количестве электронов в их электронных оболочках. Анионы обычно имеют больше электронов, чем протонов, и, следовательно, негативный заряд. Катионы, напротив, имеют меньше электронов и более положительный заряд.
Кроме заряда, существует и другое заметное различие между анионами и катионами — их взаимодействие с другими частицами. Анионы, благодаря своему отрицательному заряду, обладают большей аффинностью к положительным ионам или заряженным молекулам. Они притягиваются к катионам и могут образовывать ионные связи с ними. Например, хлоридный ион (Cl-) является типичным примером аниона, который может образовывать ионные связи с положительно заряженными металлами, такими как натрий (Na+).
Катионы, в свою очередь, обычно притягиваются к анионам или заряженным группам в молекулах. Они могут образовывать ионные связи с отрицательно заряженными группами, такими как карбоксилат (-COO-) или фосфат (-PO4). Примером катиона является калий (K+), который может образовывать ионные связи с отрицательно заряженными группами в органических молекулах.
Еще одно заметное различие между анионами и катионами заключается в их движении в электрических полях. Анионы обычно движутся к положительно заряженному полю, в то время как катионы движутся к отрицательно заряженному полю. Это свойство помогает использовать анионы и катионы в различных технологиях, таких как электрохимические процессы и батареи.
Анион и катион: что это?

Анион — это отрицательно заряженный ион. Он образуется, когда атом или группа атомов получает один или несколько электронов. Примерами анионов могут быть ионы хлора (Cl^-), оксида (O^2-), натрия (Na^-) и другие.
Катион — это положительно заряженный ион. Он образуется, когда атом или группа атомов теряет один или несколько электронов. Примерами катионов могут быть ионы натрия (Na^+), калия (K^+), кальция (Ca^2+) и другие.
Анионы и катионы играют важную роль в химии и биологии. Они образуются в процессе растворения солей, кислот и щелочей, и помогают в проведении электрического тока в растворах.
Таблица ниже показывает некоторые примеры анионов и катионов:
| Анионы | Катионы |
|---|---|
| Сульфат (SO42-) | Натрий (Na+) |
| Карбонат (CO32-) | Калий (K+) |
| Хлорид (Cl^) | Магний (Mg2+) |
Знание анионов и катионов помогает понять реакционные схемы и механизмы различных химических реакций, а также их влияние на свойства веществ.