Электролитическая диссоциация — процесс, когда соединение, обычно соль, разбивается на ионы в растворе. Это происходит под воздействием воды или другого растворителя, который разделяет молекулы соединения на положительно и отрицательно заряженные части. В результате образуются ионы, которые являются основными участниками химических реакций.
Нормальные соли — это соли, у которых все кислотные и щелочные остатки полностью замещены металлическими ионами.
Понимание электролитической диссоциации и нормальных солей важно для понимания множества химических процессов, включая растворение солей, электролиз и многие другие.
Что же такое электролитическая диссоциация и какими являются нормальные соли? Давайте разберемся!
Определение электролитической диссоциации
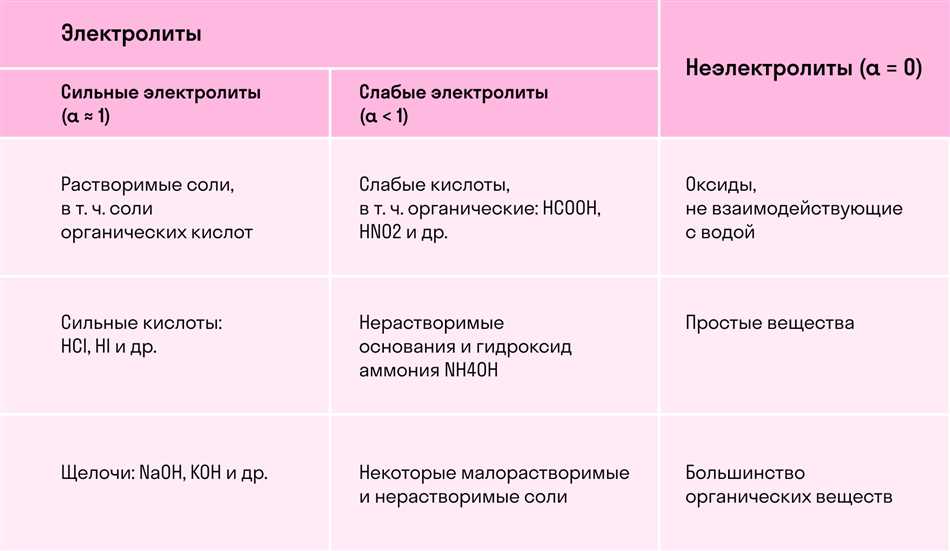
Нормальные соли являются одним из видов электролитов, которые полностью диссоциируются в водном растворе. Другими словами, каждая молекула соли расщепляется на положительное и отрицательное ионы. Например, нормальная соль натрия (NaCl) диссоциирует в Na+ и Cl- ионы.
Процесс электролитической диссоциации играет важную роль в химических реакциях, так как позволяет участвующим в реакции ионам свободно перемещаться и взаимодействовать друг с другом. Это особенно важно для электролитов, потому что они могут проводить электрический ток через раствор или плавящееся состояние.
В итоге, электролитическая диссоциация- это процесс, при котором ионные соединения расщепляются на ионы в растворе, обеспечивая проводимость электрического тока и способствуя химическим реакциям. Нормальные соли являются примером таких электролитов, которые диссоциируются полностью.
Процесс электролитической диссоциации

Когда мы растворяем соль в воде, происходит электролитическая диссоциация, и она становится электролитом. Соли, которые распадаются на ионы при диссоциации, называются нормальными солями. Например, NaCl диссоциирует на ионы натрия (Na+) и хлорида (Cl-).
Электролитическая диссоциация играет важную роль во многих процессах в химии и биологии. Она позволяет ионам перемещаться в растворе и принимать участие в химических реакциях. Кроме того, электролитическая диссоциация играет важную роль в проведении электричества в растворах и в балансе электролитов в организмах живых существ.
Таким образом, электролитическая диссоциация является ключевым процессом, который позволяет растворенным ионам свободно перемещаться и принимать участие в реакциях, что имеет большое значение как в химии, так и в биологии.
Различные виды электролитической диссоциации
Первый вид — полная электролитическая диссоциация. В этом случае соль распадается на все свои ионы, например, NaCl – распадается на Na+ и Cl-. Этот процесс происходит в водных растворах, так как вода является хорошим растворителем для ионных соединений.
Однако, есть и такие случаи, когда диссоциация происходит не полностью. Это называется частичной электролитической диссоциацией. Например, CH3COOH распадается на CH3COO- и H+. В этом случае только небольшая часть соли разлагается на ионы в растворе.
Интересно, что электролитическая диссоциация может происходить не только в водных растворах, но и в других растворителях, таких как спирт или кислород. В каждом случае процесс будет проходить по-разному, и это необходимо учитывать при изучении различных видов диссоциации.
Итак, существуют разные виды электролитической диссоциации, включая полную диссоциацию в водных растворах и частичную диссоциацию в других растворителях. Понимание этих различий помогает нам лучше понять химические процессы и их влияние на окружающую среду.
Особенности нормальных солей
Нормальные соли, в отличие от кислот и оснований, не образуют ионов ни в водных растворах, ни в чистом виде. Вместо этого, они состоят из положительно и отрицательно заряженных групп, так называемых ионов, которые привлекаются друг к другу, образуя решетку.
Все нормальные соли имеют нейтральный заряд и могут быть получены путем реакции кислоты и основания. Химическое соединение считается солью, если оно состоит из металла и неметалла, или из ионов, которые могут образовать такое соединение. Например, хлорид натрия (NaCl) — это нормальная соль, состоящая из ионов натрия (Na+) и ионов хлора (Cl-).
Нормальные соли обладают множеством удивительных свойств и широко используются в различных областях, например, в пищевой промышленности, медицине, садоводстве и многих других. Они могут быть безвредными и полезными, но также могут быть и токсичными или опасными для здоровья человека.
Нормальные соли обладают различными физическими и химическими свойствами: разным растворимостью в воде, реакцией с кислотами и основаниями, влиянием на pH растворов и т. д. Изучение свойств нормальных солей является важной задачей в химии и помогает нам лучше понять их роль и применение в различных сферах жизни.
Примеры нормальных солей

Электролитическая диссоциация — это процесс, при котором молекулы определенного вещества (электролита) разделяются на ионы, обычно под воздействием воды. Электролиты могут быть кислотами, основаниями или солями.
Теперь перейдем к нормальным солям. Нормальные соли образуются в результате реакции между кислотами и основаниями, где кислота отдает один или несколько протонов, а основание принимает эти протоны.
Есть такие классические примеры нормальных солей, о которых хочется поговорить. Например, натрий хлорид — обычная кухонная соль, которую мы применяем в ежедневной жизни для улучшения вкуса пищи. Еще один пример — серная кислота, которая может образовать сульфат натрия, широко применяемого в медицине.
А как насчет кальция? Этот элемент может образовывать соль с ацетатом — ацетат кальция. Он используется, например, в производстве пищевых добавок для укрепления костей и зубов. И задумывался ли ты о цинке? Он может образовывать сульфат цинка — необходимую соль для производства многих лекарственных препаратов.
Вот такие вот примеры нормальных солей. Их создание и использование являются важными элементами нашей повседневной жизни, либо они важны для различных отраслей промышленности и медицины.
Причины использования нормальных солей
1. Использование в лабораториях и в промышленности: Нормальные соли широко используются в химических и физических исследованиях, а также в промышленности. Они служат основными компонентами для производства различных химических продуктов, как реактивы, катализаторы и ингредиенты для производства других соединений.
2. Очистка воды и производство пищевых продуктов: Вода может содержать различные примеси и загрязнители, которые могут быть опасными для здоровья. Использование нормальных солей в процессе очистки воды помогает удалять эти примеси и обеспечивать безопасную питьевую воду. Кроме того, нормальные соли часто используются в производстве пищевых продуктов, таких как маринады, консервы и добавки.
3. Медицина и фармацевтика: Множество лекарственных препаратов содержат нормальные соли в качестве активных ингредиентов. Они играют важную роль в фармацевтической индустрии и используются для лечения различных заболеваний. Кроме того, они также используются при производстве медицинских расходных материалов и электролитических растворов для внутривенного введения.
В целом, нормальные соли играют важную роль в различных областях нашей жизни, от промышленности до медицины. Их широкое использование обусловлено их химическими свойствами и способностью выполнять различные функции в различных процессах.