Когда речь заходит о химии органических соединений, изомерия является одной из наиболее интересных и важных концепций. Концепция изомерии заключается в том, что соединения с одинаковым химическим составом, но различной структурой, называются изомерами.
Одним из видов изомерии является изомерия углеродного скелета. Она возникает, когда молекулы органических соединений отличаются по пространственному расположению и/или последовательности углеродных атомов в своих молекулах.
- Примеры изомерии углеродного скелета
- Изомерия углеродного скелета: что это такое?
- Основное понятие изомерии углеродного скелета
- Значение изомерии углеродного скелета в химических реакциях
- Примеры изомерии углеродного скелета
- Цепная изомерия
- Позиционная изомерия
- Заключение
- Вопрос-ответ:
- Что такое функциональная изомерия?
- Какие примеры функциональной изомерии можно привести?
- Как функциональная изомерия влияет на свойства органических соединений?
Примеры изомерии углеродного скелета
Хорошим примером изомерии углеродного скелета являются изомеры бутана. Бутан имеет четыре углеродных атома, поэтому можно создать несколько различных пространственных аранжировок этих атомов. В результате получаются изомеры, которые имеют различные физические и химические свойства.
Другим примером изомерии углеродного скелета являются изомеры гексана. Гексан — это соединение, которое состоит из шести углеродных атомов. Опять же, возможны разные комбинации их пространственного расположения, что приводит к образованию нескольких изомеров гексана, каждый из которых обладает собственными характеристиками и свойствами.
Изомерия углеродного скелета: что это такое?
Когда я впервые услышал о изомерии углеродного скелета, я подумал: «Как это возможно? Как молекулы могут быть одинаковыми, но при этом разными?». Однако, когда я изучил некоторые примеры, стало понятно, что это вполне нормальное явление.
Давайте рассмотрим пример. Возьмем молекулу пропана и молекулу изобутана. Обе молекулы состоят из трех атомов углерода и восьми атомов водорода. Однако, в пропане углеродные атомы расположены в виде прямой цепи, в то время как в изобутане один из углеродных атомов присоединен к остальным двум ветвями.
Таким образом, пропан и изобутан являются изомерами углеродного скелета. И это только один пример. В мире существует множество различных изомеров, каждый со своей уникальной структурой и свойствами.
Изомерия углеродного скелета — это прекрасный пример того, как при одинаковом наборе элементов можно создать различные соединения. Она показывает, как химические соединения могут быть разнообразными, открывая перед нами удивительный мир возможностей и открытий.
Основное понятие изомерии углеродного скелета
Изомерия углеродного скелета является фундаментальным понятием в органической химии и имеет широкое применение при изучении строения и свойств органических соединений.
Например, бутан и 2-метилпропан являются изомерами углеродного скелета, так как у них одинаковое химическое состав, но отличается структура их углеродных скелетов. Оба соединения состоят из 4-ех атомов углерода и 10-и атомов водорода, но бутан имеет прямую цепь углеродов, в то время как 2-метилпропан имеет ветвящуюся структуру с одним метильным (CH3) подставленным углеродным атомом.
Значение изомерии углеродного скелета в химических реакциях
Значение изомерии углеродного скелета в химических реакциях не может быть недооценено. Практически все органические соединения, такие как углеводороды, алкены, алкины, алканы и другие, обладают изомерией углеродного скелета.
Изомеры могут иметь различные физико-химические свойства и реакционную способность. Например, изомеры могут иметь различные температуры кипения, плотности, растворимости и степени окраски. Это означает, что различные изомеры могут вести себя по-разному в различных физических и химических условиях.
Изомерия углеродного скелета также играет важную роль в промышленности и в нашей повседневной жизни. Например, изомеры могут использоваться в процессе синтеза лекарственных препаратов и других химических соединений. Это позволяет достичь желаемых физиологических или химических свойств, а также улучшить эффективность и безопасность продуктов.
Таким образом, изомерия углеродного скелета является важным концептом в органической химии, влияющим на свойства и реакционные способности молекул. Понимание и использование изомерии позволяет нам разрабатывать новые соединения и улучшать существующие, внося важный вклад в различные сферы нашей жизни.
Примеры изомерии углеродного скелета
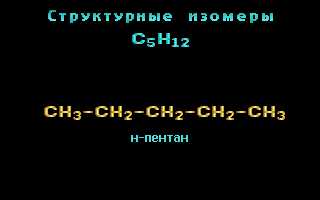
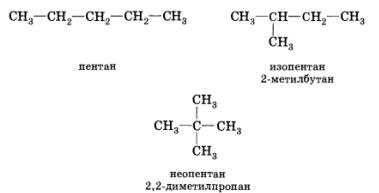
Одним из примеров изомерии углеродного скелета является изомерия цепи. В органических молекулах, содержащих несколько атомов углерода, атомы могут быть связаны в различных порядках. Например, для молекулы пентана (C5H12) существуют три основных изомера: нормальный пентан, 2-метилбутан и 2,2-диметилпропан. В нормальном пентане углеродные атомы образуют прямую цепь, в то время как в 2-метилбутане один из углеродных атомов связан с углеродом третьего уровня, и 2,2-диметилпропан имеет ветвь из двух метильных групп.
Другим примером изомерии углеродного скелета является изомерия функциональной группы. Она возникает, когда функциональные группы в молекуле размещены в разных местах. Например, в альдеграх и кетонах функциональная группа карбонил и атомы углерода могут находиться в разных позициях. Например, ацетон и пропион есть изомеры углеродного атома. В ацетоне карбонильный углерод находится в центре молекулы, а в пропионе он находится на конце цепи.
Таким образом, изомерия углеродного скелета является важным явлением в органической химии. Она позволяет узнать о разнообразии структур и свойств органических соединений и имеет большое значение для понимания химических реакций и их механизмов.
Цепная изомерия
Прежде всего, давайте вспомним, что такое углеродный скелет. Это просто описание порядка и связей атомов углерода в молекуле. В органической химии углеродные атомы могут образовывать длинные цепочки, кольца или их комбинации, что и определяет различные структуры и свойства органических соединений.
Например, в молекуле пропана (C3H8) углеродные атомы образуют прямую цепь, а в молекуле изобутана (C4H10) углероды формируют ветви. В результате, эти два соединения могут быть названы изомерами, так как они имеют одинаковую суммарную формулу, но различаются в устройстве углеродного скелета.
Часто цепные изомеры имеют разные физические и химические свойства. Это связано с тем, что разные углеродные скелеты создают фундаментально разную структуру молекулы, влияющую на взаимодействие со своим окружением.
Важно понимать, что цепная изомерия является только одним из видов изомерии, и существуют также геометрическая изомерия, оптическая изомерия и др. Комбинация этих видов изомерии обеспечивает разнообразие органических соединений в мире!
Позиционная изомерия
Когда мы слышим слово «изомерия», мы часто думаем о различных структурах молекул, а в случае позиционной изомерии речь идет именно об этом. Расположение атомов может варьироваться на различных участках молекулы, что может привести к изменению свойств соединений. Например, в гексане (C6H14) есть несколько позиционных изомеров: н-гексан, изо-гексан, гексилциклогексан.
Позиционная изомерия может влиять на реакционную способность молекулы и ее физические свойства, такие как точка плавления и кипения. Например, у изо-гексана намного ниже точка кипения, чем у н-гексана, что делает его более подходящим для использования в бензинах, поскольку он легко испаряется.
Таким образом, позиционная изомерия является важным понятием в химии органических соединений, которое помогает нам понять, как различные структуры молекул могут влиять на их свойства и применения в различных отраслях науки и промышленности.
Заключение
Функциональная изомерия обусловлена тем, что углеродные атомы в органических молекулах могут образовывать различные связи с другими атомами, такими как атомы кислорода, азота, серы и т.д., что ведет к образованию различных функциональных групп. Эти функциональные группы придают молекуле свои специфические свойства и способность участвовать в различных химических реакциях.
Примеры функциональной изомерии включают альдегиды и кетоны, амин и оксимы, эфиры и эпоксиды, карбоновые кислоты и их эстеры, амиды и соединения со спиртами. Эти различные формы функциональной изомерии могут иметь различные биологические действия и применяются в фармацевтической и пищевой промышленности.
- Важно помнить, что при изучении функциональной изомерии необходимо учитывать не только различные химические и физические свойства функциональных групп, но и их взаимодействия с другими компонентами системы.
- Функциональная изомерия является неотъемлемой частью изучения органической химии и важным элементом в разработке новых лекарственных препаратов и материалов с определенными свойствами.
Вопрос-ответ:
Что такое функциональная изомерия?
Функциональная изомерия — это явление, при котором у различных органических соединений одна и та же молекулярная формула, но разные функциональные группы или типы связей.
Какие примеры функциональной изомерии можно привести?
Примеры функциональной изомерии включают альдегиды и кетоны, эфиры и карбоновые кислоты, амиды и нитрилы, а также много других сочетаний функциональных групп.
Как функциональная изомерия влияет на свойства органических соединений?
Функциональная изомерия может оказывать значительное влияние на свойства органических соединений. Например, различные функциональные группы могут влиять на их реакционную способность, степень насыщенности и температуры плавления и кипения.