Давайте рассмотрим примеры изомеров. Один из самых известных случаев изомерии — это бензол и циклогексан. Оба соединения имеют формулу C6H6, но структурно они различаются. Бензол представляет собой плоское кольцо ароматических атомов углерода, в то время как циклогексан образует шестиугольное кольцо алифатических атомов углерода. Таким образом, хотя их формулы одинаковы, их свойства и реакции совершенно различны.
Изомерия — это удивительное явление, которое демонстрирует многообразие химических соединений. Исследование изомеров позволяет нам лучше понять строение и свойства различных веществ, что важно как для науки, так и для промышленности.
Что такое изомеры?
Давайте рассмотрим пример, чтобы лучше понять, что это значит. Возьмем два изомера пропана: нормальный пропан (CH3-CH2-CH3) и изо пропан (CH3-CH(CH3)2). Оба изомера имеют одинаковую химическую формулу C3H8, но они отличаются внутренним расположением атомов. У нормального пропана атомы углерода связаны последовательно, в то время как у изо пропана один из атомов углерода связан с другими двумя атомами углерода, образуя ветвь. Это различие в структуре делает разницу в их свойствах, таких как температура кипения и плотность.
Изомеры встречаются в различных областях химии, включая органическую и неорганическую химию, и они имеют важное значение для понимания структуры и свойств химических соединений.
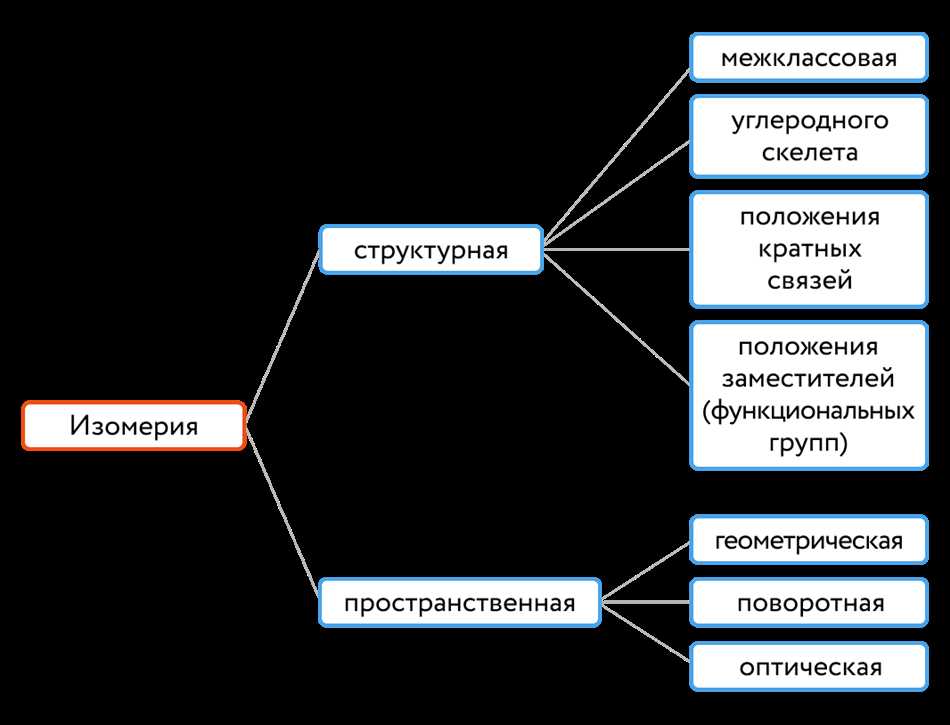
Структурные изомеры
Примерами структурных изомеров могут служить молекулы этиленгликоля и пропанола. Оба они имеют химическую формулу C3H8O, но их атомы расположены по-разному. У этиленгликоля два атома углерода связаны атомами кислорода, а у пропанола один атом углерода соединен с атомами кислорода и водорода.
- Этиленгликоль: CH2(OH)-CH2(OH)
- Пропанол: CH3-CH2-OH
Эти примеры показывают, как маленькое изменение в расположении атомов может привести к образованию разных структурных изомеров. Структурные изомеры могут иметь различные свойства и реакционную способность, что делает их важными в химической науке и промышленности.
Изомерия геометрическая
Вы знали, что химические соединения могут иметь одинаковую химическую формулу, но различную пространственную структуру? Именно такая разновидность изомерии и называется геометрической изомерией.
Ладно, представьте себе это: у вас есть два плоских веера, и вы можете по-разному их перекладывать. Вот так же происходит и с геометрическими изомерами. Они отличаются расположением атомов или групп атомов в пространстве.
Рассмотрим пример: изомерия геометрическая проявляется в случае, когда связи между атомами углерода отличаются только по пространственному расположению. Например, изомеры геометрические можно обнаружить в алкенах. При этом эти изомеры могут обладать разными физическими и химическими свойствами.
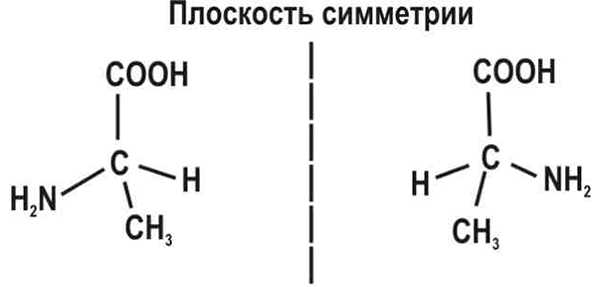
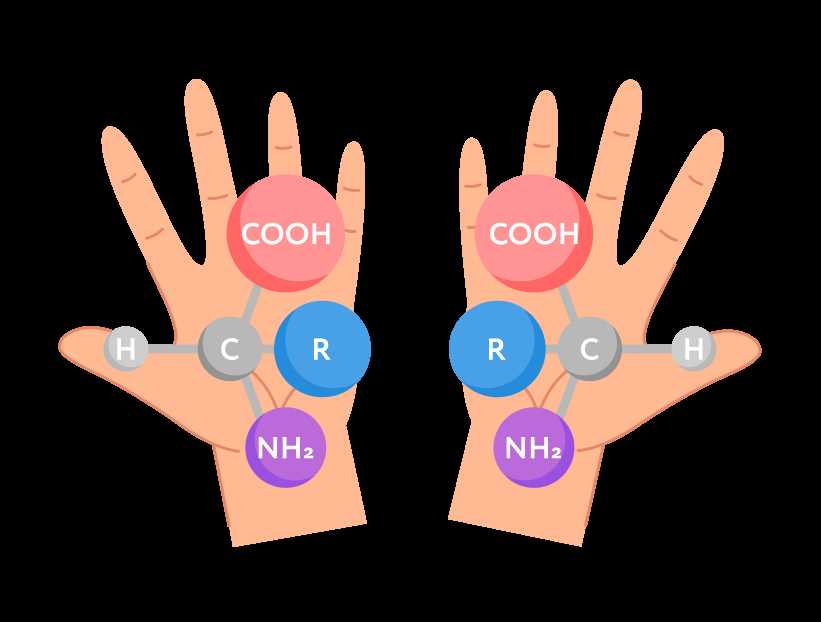
Изомерия Оптическая
Огромное количество органических соединений обладает такими изомерами и это дает нам понять, насколько сложен мир химии. Например, одно из самых известных оптических изомеров — это D-глюкоза и L-глюкоза. Они оба состоят из шести атомов углерода, двенадцати атомов водорода и шести атомов кислорода, но имеют разное строение.
Изомерия оптическая играет важную роль в биохимии и фармакологии. Например, имеется такой факт: один оптический изомер может быть лекарственным препаратом, а другой может быть токсическим или неактивным.
Поэтому изучение изомерии оптической является важным шагом для разработки новых лекарственных препаратов и понимания процессов, происходящих в нашем организме. Удивительно, правда? Узнать больше о роли изомерии оптической в нашей жизни можно продолжать исследовать и учиться в мире химии.
Заключение
Мы рассмотрели примеры структурной изомерии, к которой относятся геометрическая, цепная и групповая изомерия. Каждый из типов изомерии имеет свои характерные признаки и может влиять на свойства и реакционную способность молекулы.
Также мы рассмотрели примеры функциональной изомерии, где различие в свойствах и реактивности обусловлено различным функциональным группировкам в молекуле. Такие изомеры могут иметь совершенно разные свойства и использоваться в различных областях химии и промышленности.
Изучение изомерии является важной задачей органической химии, так как позволяет понять строение и свойства различных соединений, а также предсказать их поведение в различных реакциях. Знание основных примеров изомеров является фундаментальным для понимания и развития органической химии в целом.
Вопрос-ответ:
Что такое изомеры?
Изомеры – это соединения, которые имеют одинаковую молекулярную формулу, но различную структуру или пространственное расположение атомов. То есть, изомеры могут иметь разные свойства и реакционную способность, несмотря на одинаковый химический состав.
Существуют ли примеры изомеров в органической химии?
Да, примеры изомеров в органической химии очень распространены. Например, бутилен и изобутилен – это изомеры углеводородов с молекулярной формулой C4H8. Или же ацетон и пропанон – изомеры с молекулярной формулой C3H6O. В органической химии очень много изомеров, так как они могут иметь различные организационные структуры и пространственное расположение своих атомов.
Каковы примеры изомеров в неорганической химии?
В неорганической химии также есть примеры изомеров, но они встречаются не так часто, как в органической химии. Например, гексахлороциклогексан и гексахлороциклопентадиен – это изомеры с молекулярной формулой C6H6Cl6. Вне органической химии примеры изомеров могут быть более сложными и редкими, но все же они существуют.