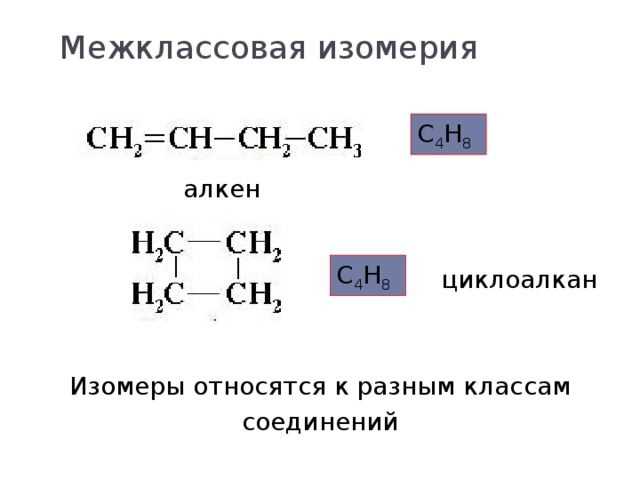
Слышали ли вы когда-нибудь о понятии «изомеры» в химии? Если нет, то не беспокойтесь, я объясню вам, о чем речь. Изомеры — это вещества, которые обладают одинаковым химическим составом, но различаются в своей структуре. Другими словами, они имеют одинаковое количество атомов разных элементов, но разные способы, которыми эти атомы связаны друг с другом.
Изомеры могут отличаться в физических свойствах, например, в температуре плавления и кипения, а также в химических свойствах, например, взаимодействии с другими веществами. Благодаря этим отличиям, изомеры могут обладать различными свойствами и применяются в различных сферах, начиная от фармацевтической индустрии до производства пищевых продуктов.
Вот такими простыми словами можно описать таинственный мир изомеров в химии. В следующий раз, услышав это слово, вы уже будете знать, что имеется в виду.
- Раздел 1: Краткое понятие об изомерии
- Раздел 2: Основные типы изомеров
- Структурные изомеры
- Изомерия функциональных групп
- Изомерия геометрических изомеров
- Раздел 3: Структурные изомеры
- Раздел 4: Функциональные изомеры
- Раздел 5: Геометрические изомеры
- Раздел 6: Определение и классификация изомеров
- Раздел 7: Примеры изомерии в химии
- 1. Изомеры цепей углерода
- 2. Оптическая изомерия
- 3. Геометрическая изомерия
- 4. Грузовая и строительная изомерия
Раздел 1: Краткое понятие об изомерии
Можете представить изомерию как разновидность химического пазла. Представьте себе, что у вас есть один набор атомов, но вы можете их расставлять в разных комбинациях и получать разные изомеры. Вот и все! Просто менее техническое определение изомерии.
Так как изомеры имеют различную структуру, они имеют различные химические и физические свойства. Некоторые изомеры могут быть более реакционноспособными, другие — более стабильными. Изомерия также может играть важную роль в фармацевтической и органической химии, так как различные изомеры могут обладать различными лечебными свойствами.
Интересно, верно? А что если я скажу вам, что изомерия имеет глубокие фундаментальные основания в самой природе вещества? Ответ на этот вопрос мы подробнее рассмотрим в следующем разделе.
Раздел 2: Основные типы изомеров
Структурные изомеры
Первый тип изомерии, о котором я хотел бы поговорить, — это структурные изомеры. Они отличаются по своей структуре, то есть атомы располагаются по-разному, но все еще имеют ту же химическую формулу. Например, пентан и 2-метилбутан являются структурными изомерами, так как у них разное расположение атомов углерода.
Изомерия функциональных групп
Следующий тип изомерии — это изомерия функциональных групп. Здесь различия связаны с наличием или расположением функциональных групп в молекуле. Например, альдегид и кетон являются изомерами функциональных групп, так как они имеют разные функциональные группы — спиртовую и кетоновую соответственно.
Изомерия геометрических изомеров
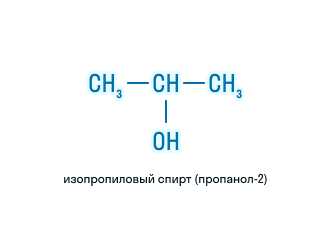
Геометрическая изомерия — третий тип изомерии, о котором стоит узнать. Этот тип изомерии связан с различным расположением заместителей вокруг двойной связи или цикла. Например, цис-бутадиен и транс-бутадиен являются геометрическими изомерами, так как у них разное расположение заместителей вокруг двойной связи.
Таким образом, есть несколько основных типов изомеров, которые можно увидеть в химии. Эти изомеры имеют различную структуру, функциональные группы и геометрию, но все они являются разными формами одного и того же химического соединения.
Раздел 3: Структурные изомеры
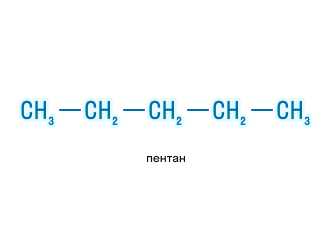
Давайте представим, что у нас есть два разных способа размещения атомов углерода и водорода в молекуле. Мы получим два структурных изомера. Например, метан и этилен. Они оба состоят из одного атома углерода и четырех атомов водорода, но в этилене два атома углерода объединены двойной связью, в то время как в метане атомы углерода связаны одиночной связью.
Еще один пример — это изомеры альдегидов и кетонов. Оба класса химических соединений содержат группу карбонильного соединения (C=O), но в альдегидах карбонильная группа находится на конце молекулы, в то время как в кетонах она находится в середине.
Важно понимать, что структурные изомеры обладают различными свойствами и обычно обусловливают различное химическое поведение. Это делает изучение структурных изомеров важным и интересным аспектом химии.
Раздел 4: Функциональные изомеры
Давай посмотрим на пример. У нас есть две молекулы – этанол и этер. Они обе состоят из двух атомов углерода, шести атомов водорода и одного атома кислорода.
| Молекула | Структурная формула |
|---|---|
| Этанол | H3C—C2H5O+ |
| Этeр | 3C—O—C2H5 |
У этанола есть гидроксильная (ОН) группа, а у этера ее нет. Вот и вся разница! Несмотря на одинаковое количество атомов, эти молекулы имеют разные свойства и используются по-разному. Этанол, например, можно использовать в качестве растворителя или для приготовления алкогольных напитков, а этер используется как растворитель в лакокрасочной промышленности.
Так что, у функциональных изомеров может быть разная химическая активность и разные применения. Интересно, какая же группа будет в дальнейшем применении?
Раздел 5: Геометрические изомеры
Давай представим, что у нас есть два человека, у которых одинаковые черты лица, но один из них носит очки, а второй — нет. Вот так и с геометрическими изомерами. Есть одна молекула, но атомы в ней могут быть сложены по-разному.
Один из примеров геометрических изомеров — это цис- и транс-изомеры. В цис-изомере атомы или группы атомов связаны между собой с одной стороны, а в транс-изомере — с противоположной стороны. Да, это звучит непросто, но давай посмотрим на примере.
- Допустим, у нас есть молекула с черным атомом и двумя белыми атомами, которые связаны друг с другом.
- Если белые атомы находятся с одной стороны черного атома, это будет цис-изомер.
- Если же белые атомы находятся с противоположной стороны, это будет транс-изомер.
Интересно, правда? Геометрические изомеры могут иметь разные свойства и свои уникальные особенности. Их изучение помогает нам лучше понять мир химии и создавать новые вещества с нужными свойствами.
Раздел 6: Определение и классификация изомеров
Изомеры можно классифицировать на несколько типов. Например, существуют структурные изомеры, которые отличаются отличаются молекулярной структурой. Некоторые из них могут иметь различные расположение функциональных групп, а другие могут иметь различное количество атомов внутри молекулы.
Другой тип изомеров — геометрические изомеры. Они отличаются отличаться конфигурацией атомов в пространстве. Например, у них могут быть разные углы связей или различные атрибуты вращения.
Еще один тип изомеров — оптические изомеры. Они отличаются отличаться способностью поворота плоскости поляризации света. Некоторые изомеры могут поворачивать свет влево, а другие — вправо.
Все эти классификации помогают ученым лучше понять и систематизировать различные формы изомерии. Знание о существовании изомеров позволяет химикам лучше понять химические реакции и свойства веществ, а также использовать их в промышленности и медицине.
Раздел 7: Примеры изомерии в химии
1. Изомеры цепей углерода
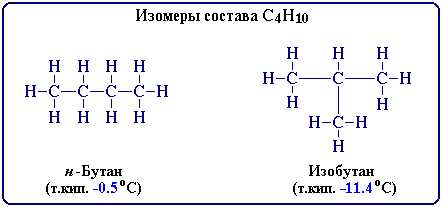
Примером изомерии цепей углерода являются н-бутан и изобутан. Оба изомера содержат 4 атома углерода, но их устройство отличается. Н-бутан имеет прямую цепь из 4 углеродных атомов, тогда как изобутан имеет ветвь из 3 углеродных атомов. Из-за этого у изобутана есть дополнительные возможности для молекулярного движения, что влияет на его физические и химические свойства.
2. Оптическая изомерия
Оптическая изомерия относится к явлению, когда молекулы имеют одинаковую форму и связи, но отличаются ориентацией групп вокруг асимметричного атома. Примером таких изомеров являются D-глюкоза и L-глюкоза. Оба изомера состоят из 6 атомов углерода и имеют одинаковую форму, но они отличаются только ориентацией гидроксильных групп вокруг асимметричного углерода. Это влияет на их взаимодействие с другими молекулами и их биологическую активность.
3. Геометрическая изомерия
Геометрическая изомерия возникает, когда молекулы имеют одинаковое количество и тип связей, но отличаются пространственным расположением атомов. Примером геометрической изомерии являются изомеры бутена. У cis-изомера два метильных заместителя находятся на одной стороне двойной связи, а у trans-изомера — на противоположных сторонах. Из-за этого они имеют различные физические и химические свойства.
4. Грузовая и строительная изомерия
Грузовая и строительная изомерия относятся к случаям, когда атомы имеют разное порядковое расположение в молекуле. Примером таких изомеров являются метан и метиламин. Метан имеет один углеродный атом и четыре атома водорода, тогда как метиламин содержит один углеродный атом, два атома водорода и один атом азота. Их различная структура обусловливает различные свойства и возможности для взаимодействия с другими веществами.
Выше приведены только некоторые примеры изомерии в химии. Это явление имеет множество проявлений и может быть наблюдаемо в различных классах органических и неорганических соединений. Изучение изомерии важно для понимания структуры и свойств химических соединений, а также для их применения в различных областях науки и технологии.




