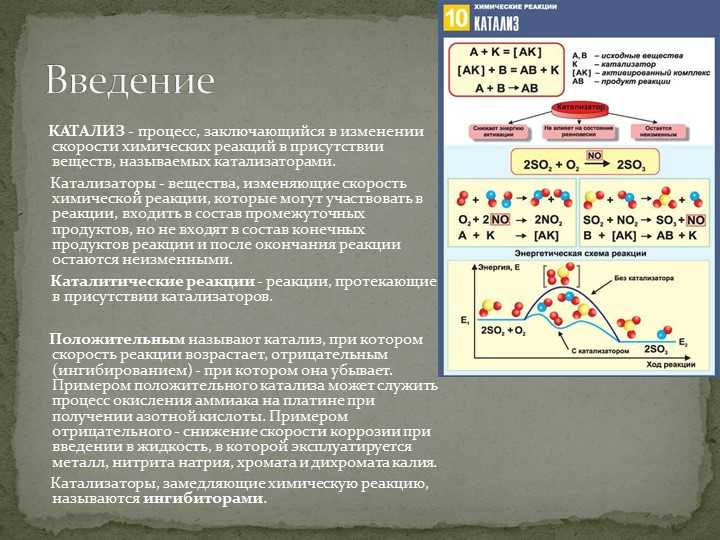
Катализатор — это вещество, которое ускоряет химическую реакцию, не затрачиваясь при этом полностью. Он играет важную роль во многих химических процессах, обеспечивая эффективность и экономию ресурсов. Катализаторы могут быть естественными или искусственными веществами, их тип и свойства зависят от конкретной реакции, в которой они применяются.
Молекулы катализатора активно участвуют в промежуточных стадиях реакции, снижая активационную энергию и помогая образованию продукта. Благодаря этому, катализаторы позволяют увеличить скорость и селективность реакции, снизить температуру и давление необходимые для ее проведения. Их использование обеспечивает более эффективное использование сырья, снижает энергозатраты и сокращает вредные выбросы в окружающую среду.
- Катализаторы: определение и роль в химических процессах
- Что такое катализаторы?
- Зачем нам нужны катализаторы?
- Принцип работы катализаторов
- Виды катализаторов
- Гетерогенные катализаторы
- Гомогенные катализаторы
- Энзимные катализаторы
- Фотокатализаторы
- Применение катализаторов
- Катализатор: определение и роль в химических процессах
- Роль катализаторов в химии
Катализаторы: определение и роль в химических процессах
Когда мы слышим слово «катализатор», сразу в голову приходят ассоциации с неотъемлемой частью химических процессов. Но что это такое на самом деле и какова их роль в химии?
Катализаторы — это вещества, которые повышают скорость химических реакций, не расходуясь при этом. Они являются своеобразными «помощниками» в химических процессах и позволяют им происходить гораздо быстрее, чем они происходили бы без их участия.
Представьте, что у вас есть задача решить определенную проблему, но у вас нет необходимых навыков или инструментов для ее решения. В этом случае вы бы обратились к человеку, который обладает нужными навыками или использовали бы подходящий инструмент, чтобы выполнить задачу быстро и эффективно. Точно так же и катализаторы в химических процессах — они ускоряют и облегчают химические реакции, необходимые для образования новых веществ.
Интересно отметить, что катализаторы не только ускоряют реакции, но также могут изменять сами реакции. Они могут позволить реакции происходить при более низких температурах и давлениях, что экономически выгодно, так как требует меньшего количества энергии и ресурсов. Катализаторы также могут быть использованы для создания более эффективных и экологически чистых процессов.
Как мы видим, роль катализаторов в химических процессах нельзя недооценивать. Они играют важную роль в повышении эффективности и энергонезависимости химической промышленности. Благодаря катализаторам мы можем получать нужные нам продукты быстрее и дешевле, что является неотъемлемой частью нашей современной жизни.
Что такое катализаторы?
Вот представьте, вы это выходите на пробежку, и вам легко и удобно бежать одному. Но что, если вы бы смогли взять с собой специального тренера, который будет вас подбадривать, указывать на ошибки и наставлять, как преодолевать сложные участки? Ваша эффективность и продуктивность в беге значительно возрастут, не правда ли?
Точно так же работают катализаторы в химических реакциях. Они ускоряют скорость реакции, уменьшают активационную энергию, стимулируют взаимодействие между частицами реагентов и помогают получить желаемые продукты. Это особенно важно, когда реакция без катализатора протекала бы слишком медленно или вообще не происходила бы.
Зачем нам нужны катализаторы?
Катализаторы сыграли огромную роль в развитии нашей цивилизации, потому что они позволили нам ускорить процессы производства и улучшить качество продуктов. Благодаря катализаторам, мы можем:
- Сократить затраты энергии и времени, что позволяет производить больше товаров в короткие сроки.
- Улучшить качество продуктов, исключая побочные или нежелательные реакции.
- Экономить сырье, перерабатывая его более полно и эффективно.
- Улучшить безопасность процессов, уменьшив риск возникновения опасных ситуаций.
Кроме того, катализаторы являются ключевым элементом поиска новых, более экологически чистых процессов производства. Они помогают снизить выбросы вредных веществ в атмосферу и охранять наше окружающую среду. Таким образом, они играют важную роль в создании устойчивого развития и заботы о будущем поколении.
Теперь вы понимаете, какой невероятный эффект катализаторы могут оказывать на химические процессы. Они превращают сложные и медленные реакции в быстрые и эффективные, делая мир краше и лучше. Получается, что эти волшебники химии являются одной из ключевых составляющих нашей современной жизни. Используем их мудро и благодарно, чтобы создавать более прогрессивное и устойчивое будущее.
Принцип работы катализаторов
Катализаторы играют ключевую роль в химических процессах, их основной принцип работы заключается в ускорении химических реакций без влияния на саму реакцию. Иными словами, они позволяют перейти от одного состояния вещества к другому, не участвуя в реакции непосредственно, но ускоряя ее и упрощая процесс.
Когда две молекулы сталкиваются друг с другом, их атомы воздействуют друг на друга, изменяют их связи и формируют новые вещества. Однако, эта перестройка атомов может быть сложным процессом, требующим времени и энергии. В этот момент на помощь приходят катализаторы.
Основное достоинство катализаторов состоит в том, что они снижают энергию активации, необходимую для того, чтобы реакция началась. Они предоставляют молекулам возможность искать реакционные пути, которые были бы недоступны без их присутствия, и активируют необходимые переходы.
Работа катализатора можно представить как вспомогательную руку на пути молекул к образованию новых соединений. Он может предложить опору и направление, помочь молекуле сориентироваться в нужном направлении и преодолеть энергетический барьер.
Процесс работы катализаторов аналогичен работе гимнаста на брусьях. Гимнаст, используя брусья как поддержку, может выполнить сложные движения, которые были бы нереальны без поддержки. Точно так же, в присутствии катализатора, молекулы могут проходить через сложный реакционный путь с меньшей энергией и большей эффективностью.
Катализаторы могут быть различных типов — металлическими, органическими, биологическими и другими, в зависимости от химической реакции, которую они ускоряют. Они используются в промышленности, медицине, сельском хозяйстве и других областях, где происходят химические превращения.
Итак, принцип работы катализаторов основывается на способности этих веществ ускорять химические реакции путем снижения энергии активации. Они помогают молекулам найти пути, которые обеспечивают более эффективное и быстрое образование новых соединений. Использование катализаторов в различных сферах науки и технологий позволяет создавать новые продукты, оптимизировать процессы и снижать негативное воздействие на окружающую среду.
Виды катализаторов
Катализаторы играют ключевую роль в химических процессах, ускоряя реакции, снижая температуры и повышая эффективность. Существует несколько различных видов катализаторов, каждый из которых выполняет свою специфическую функцию.
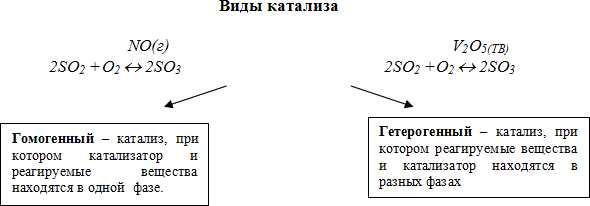
Гетерогенные катализаторы
Гетерогенные катализаторы — это катализаторы, которые физически разделяются от реагентов в процессе реакции. Они обычно существуют в форме твердых частиц или поверхностей, как, например, металлы или оксиды металлов. Гетерогенные катализаторы широко применяются в промышленности для изготовления различных химических продуктов, таких как аммиак, нефтепродукты и пластик.
Гомогенные катализаторы
Гомогенные катализаторы — это катализаторы, которые находятся в одной фазе с реагентами. Они обычно представлены химическими соединениями, такими как кислоты или металлокомплексы, которые способны активировать реагенты и ускорять реакции. Гомогенные катализаторы широко используются в органической химии и синтезе полимеров.
Энзимные катализаторы

Энзимные катализаторы — это белки, которые катализируют реакции в живых системах. Они играют решающую роль в биохимических процессах и метаболизме. Энзимы специфичны по отношению к реакциям, которые они ускоряют, и могут быть использованы в промышленности для производства витаминов, пищевых добавок и лекарственных препаратов.
Фотокатализаторы
Фотокатализаторы — это катализаторы, которые активируются при воздействии света. Они используются, например, для разложения загрязняющих веществ в воздухе и воде с помощью фотокаталитической реакции. Фотокатализаторы могут быть органическими или неорганическими веществами и играют важную роль в фотохимических процессах.
Принципиально важно то, что катализаторы ускоряют химические реакции, не изменяя самих себя. Это позволяет им быть эффективными и долговечными инструментами для современной химии и промышленности. Каждый из типов катализаторов обладает своими особенностями и применяется в различных областях науки и технологий.
Применение катализаторов
Катализаторы широко применяются в химической промышленности и в различных химических процессах. Их роль заключается в ускорении химических реакций, снижении энергозатрат и повышении эффективности процессов.
Один из наиболее распространенных примеров применения катализаторов в промышленности — это производство аммиака с использованием катализатора из железа и малышей. Аммиак является важным сырьем для производства удобрений, пластмасс, красителей и других химических продуктов. Без катализатора процесс получения аммиака был бы очень медленным и неэффективным.
Катализаторы также применяются в процессах гидрогенизации, которые используются для производства многих продуктов, включая нефть, пластмассы, синтетические материалы и даже пищевые продукты. Гидрогенизация — это процесс добавления водорода к молекуле вещества с целью изменения его химических свойств. Катализаторы, такие как никель или платина, помогают ускорить этот процесс и снизить температуру и давление, необходимые для его проведения. Это позволяет сэкономить энергию и улучшить производительность.
Еще одним важным применением катализаторов является процесс каталитического крекинга, используемый в нефтеперерабатывающей промышленности. Крекинг — это процесс разделения больших молекул углеводородов на более маленькие, которые могут быть использованы для производства бензина, дизельного топлива и других нефтепродуктов. Катализаторы такие, как алюмосиликаты или зеолиты, применяемые в этом процессе, помогают ускорить реакцию и повысить выход ценных продуктов.
И это только несколько примеров. Катализаторы используются во всех отраслях промышленности, где требуется ускорение химических реакций, включая производство фармацевтических веществ, пластмасс, полимеров и катализаторов самих. Без катализаторов многие процессы просто не могли бы осуществляться или были бы слишком затратными и неэффективными.
И наконец, катализаторы играют важную роль не только в промышленности, но и в повседневной жизни. Например, катализаторы применяются в автомобилях для очистки отработавших газов, таких как оксиды азота и углеводороды, перед их выбросом в атмосферу. Катализаторы помогают снизить вредные выбросы и улучшить качество воздуха, делая нашу жизнь безопаснее и экологичнее.
Таким образом, применение катализаторов имеет огромное значение для современной промышленности и жизни в целом. Они значительно повышают эффективность и экономичность процессов, способствуют развитию новых технологий и улучшают качество окружающей среды. Без них многие из наших повседневных продуктов и удобств, которыми мы пользуемся, не существовали бы или были бы недоступны.
Катализатор: определение и роль в химических процессах
Катализаторы играют важную роль в химических процессах. Они позволяют снизить энергию активационного барьера и ускорить химическую реакцию. Благодаря катализу возможны процессы, которые при обычных условиях проходят очень медленно или не происходят вовсе.
В реакции катализатор ускоряет химическую реакцию, но сам не участвует в продуктах реакции. Он может быть использован многократно, поскольку после завершения реакции он возвращается в исходное состояние и может быть использован снова.
Катализаторы могут быть разных типов: гомогенные, которые находятся в одной фазе с реагентами, и гетерогенные, которые находятся в разных фазах. Гетерогенные катализаторы часто представляют собой поверхность, на которой происходят химические реакции.
Катализаторы широко применяются в промышленности для синтеза различных соединений, производства пластмасс, лекарств и других продуктов. Они также играют важную роль в жизни организмов, участвуя в биохимических процессах и обеспечивая нормальное функционирование клеток и органов.
Роль катализаторов в химии
- Ускорение химических реакций;
- Снижение энергии активации, необходимой для реакции;
- Повышение выхода продукта реакции;
- Получение специфических продуктов реакции;
- Экономия энергии и ресурсов в химических процессах.
Катализаторы играют важную роль в множестве химических процессов, делая их более эффективными и экономичными. Их применение позволяет получить продукты высокой чистоты и ускорить процессы, что имеет большое значение в различных отраслях промышленности и в науке.