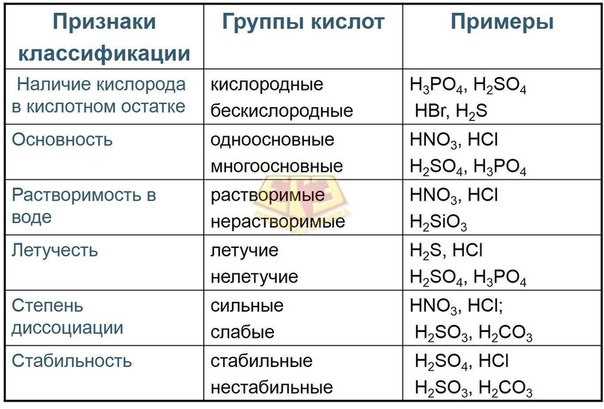
Кислоты — одни из важнейших компонентов в области химии. Они играют ключевую роль во многих процессах и реакциях, находясь в основе множества веществ. Кислоты характеризуются наличием водородных ионов, которые взаимодействуют с другими веществами, создавая новые соединения.
Кислоты встречаются в различных формах и классифицируются по разным признакам: по их силе, по их составу и по способу получения. Некоторые примеры кислот включают уксусную кислоту, серную кислоту и соляную кислоту. Узнайте больше о свойствах и применениях кислот в химической науке.
- Что такое кислоты?
- Определение кислот
- Примеры кислот
- Свойства кислот
- 1. Кислотные свойства
- 2. Реакция с щелочами
- 3. Естественное воздействие на организмы
- Заключение
- Классификация кислот
- Основание определения:
- Основание применения:
- Примеры естественных кислот
- Серная кислота (H2SO4)
- Соляная кислота (HCl)
- Солянокислый аммоний (NH4Cl)
- Фосфорная кислота (H3PO4)
- Солянокислый натрий (NaCl)
- Кислоты в химии: определение и примеры
- Примеры кислот:
Что такое кислоты?
Основное свойство кислот — их кислотность. Когда кислота растворяется в воде, она образует водородные ионы (H+). Это делает раствор кислоты кислотным, что может быть измерено с помощью pH-шкалы. Различные кислоты имеют разную степень кислотности, и pH-значение может быть меньше 7.
Кислоты могут быть органическими или неорганическими. Органические кислоты содержат углерод, а неорганические — нет. Примерами органических кислот являются уксусная кислота (находящаяся в уксусе) и лимонная кислота (находящаяся в лимонном соке). Примерами неорганических кислот являются серная кислота (используется в производстве удобрений) и соляная кислота ( использование в химической промышленности).
Одно из важных применений кислот связано с пищевой промышленностью. Многие кислоты используются как пищевые добавки для придания определенных вкусов и консистенции пищевым продуктам. К примеру, лимонная кислота добавляется в газировку для создания кислого вкуса.
Кислоты также широко используются в лабораториях для проведения химических экспериментов и анализа. Они могут быть использованы для определения содержания различных веществ в образцах, таких как пищевые продукты или вода.
Важно помнить, что хотя кислоты могут быть полезными и иметь множество применений, они также могут быть опасными. Концентрированные кислоты могут вызывать ожоги и другие вредные эффекты. Поэтому всегда важно соблюдать меры безопасности при работе с ними.
Итак, кислоты — это химические соединения, которые обладают кислотностью и имеют много применений в пищевой промышленности, лабораторных исследованиях и других отраслях. Использование кислот помогает нам в понимании химии и создании новых продуктов и технологий. Удивительно, как небольшое соединение может иметь такое большое влияние на нашу жизнь, не так ли?
Определение кислот
Кислоты — это вещества, которые, в присутствии воды, образуют ион водорода, известный как протон. Основным свойством кислот является то, что они могут отдавать этот протон другим веществам. Такой процесс называется диссоциацией. Поэтому кислоты часто называют донорами протонов.
Мы можем встретить кислоты как в природном, так и в синтетическом виде. Они могут быть жидкими, газообразными или твердыми веществами, а их свойства могут сильно отличаться. К некоторым известным ежедневным примерам кислот относятся лимонный сок, яблочный уксус и соляная кислота.
Примеры кислот
- Лимонная кислота: это одна из самых распространенных кислот, которая присутствует во многих фруктах и овощах, таких как лимоны, апельсины и грейпфруты. Она широко используется в пищевой промышленности для консервации и приготовления различных продуктов.
- Соляная кислота: это одна из самых сильных и коррозийных кислот. Она находит широкое применение в различных отраслях, включая промышленность и лабораторные исследования.
- Уксусная кислота: это кислота, которая присутствует в уксусе, используется для различных целей, таких как консервирование пищи и приготовление соусов.
- Серная кислота: это еще одна сильная кислота, которая широко используется в промышленности, включая производство удобрений и чистку металлов.
- Аскорбиновая кислота: также известная как витамин C, это кислота, которая важна для нашего здоровья и иммунной системы.
Кислоты — это удивительные вещества, которые играют важную роль в химии и повседневной жизни. Они помогают нам в пищеварении, в производстве различных продуктов и обеспечивают безопасность и санитарию в промышленности. Знание о кислотах позволяет нам лучше понять мир химии и как использовать их в нашей пользе.
Свойства кислот
1. Кислотные свойства
Одно из основных свойств кислот, вызывающее их отличие от других химических соединений, — это их кислотность. Когда кислоты растворяются в воде, они образуют положительные ионы водорода и отрицательные ионы кислотных радикалов. Это делает растворы кислот кислыми.
Кислые растворы имеют характерные свойства, такие как острый вкус и способность изменять цвет некоторых индикаторов. Например, лакмус — распространенный индикатор — обращает жидкость красной или фиолетовой при добавлении кислоты.
2. Реакция с щелочами
Другим важным свойством кислот является их реакция с щелочами. Кислоты и щелочи — две основные категории химических соединений, которые могут взаимодействовать друг с другом. Когда кислота реагирует со щелочью, они образуют соль и воду.
Например, если добавить кислоту, такую как уксус, к щелочи, такой как гидроксид натрия, произойдет реакция, которая приведет к образованию натрий ацетата и воды.
3. Естественное воздействие на организмы
Многие кислоты имеют естественное воздействие на организмы и часто используются в медицине и пищевой промышленности. К примеру, аскорбиновая кислота (витамин С) является необходимой для здоровья человека и участвует во многих жизненно важных процессах.
Однако, не все кислоты безопасны для потребления. Некоторые сильные кислоты могут вызывать ожоги и другие травмы, если они попадают на кожу или слизистые оболочки. Поэтому, кислоты должны быть использованы с осторожностью и в соответствии с инструкциями.
Заключение
Есть много свойств, которыми обладают кислоты, и эти свойства делают их уникальными в мире химии. Когда у вас возникает вопрос о том, что такое кислота или какие у нее свойства, помните, что они могут быть кислотными вкусом, реагировать с щелочами и иметь взаимодействие с организмами. Берегите себя и будьте осторожны при обращении с кислотами!
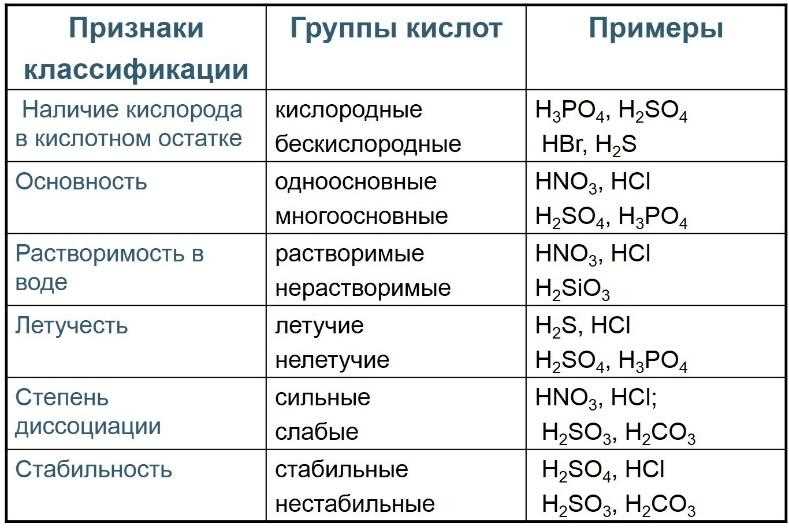
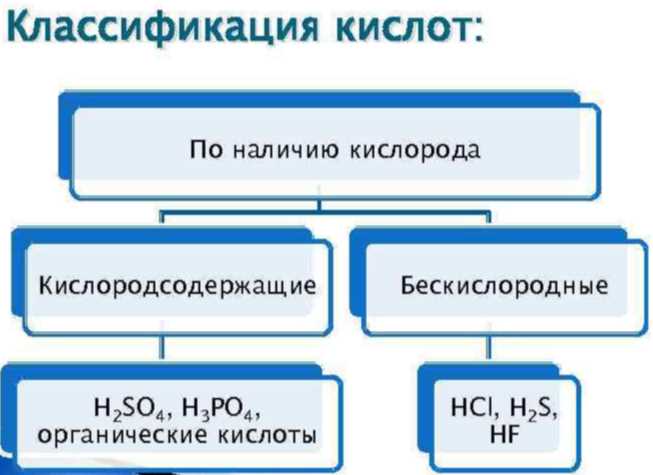
Классификация кислот
Основание определения:
- Оксидные кислоты: такие кислоты содержат атом кислорода в своей структуре. Примеры включают серную кислоту (H2SO4) и азотную кислоту (HNO3).
- Анионные кислоты: эти кислоты образуются отрицательно заряженными ионами, называемыми анионами. Примеры включают хлористоводородную кислоту (HCl) и фтористоводородную кислоту (HF).
- Бинарные кислоты: такие кислоты состоят из двух элементов, а именно водорода и другого химического элемента. Примеры включают соляную кислоту (HCl) и фосфорную кислоту (H3PO4).
- Кислоты смешанного типа: это кислоты, которые не подпадают ни под одну из вышеупомянутых категорий. Примеры включают сероводородную кислоту (H2S).
Основание применения:
- Органические кислоты: это кислоты, содержащие углерод в своей структуре. Они широко применяются в органической химии и имеют разнообразные применения, от пищевой промышленности до производства лекарств. Примеры включают уксусную кислоту (CH3COOH) и салициловую кислоту (C7H6O3).
- Неорганические кислоты: это кислоты, которые не содержат углерод в своей структуре. Они применяются в различных отраслях, включая металлургию, электронику и очистку воды. Примеры включают соляную кислоту (HCl) и серную кислоту (H2SO4).
Важно понимать, что классификация кислот — это лишь один из способов их группировки, и существуют и другие подходы к их классификации. Каждый тип кислот имеет свои уникальные свойства и применения, что делает их особенно интересными для изучения и использования в практических целях.
Примеры естественных кислот
Лимонная кислота: Одна из наиболее распространенных естественных кислот, которая придает освежающий кислый вкус цитрусовым плодам. Лимоны, лаймы и апельсины являются отличными источниками лимонной кислоты. Эта кислота широко используется в пищевой промышленности для консервации и придания кислотности различным продуктам.
Уксусная кислота: Это естественная кислота, которая присутствует в уксусе. Уксусная кислота имеет резкий запах и острый вкус и широко используется для приготовления соусов и маринадов. Она также является одним из основных компонентов уксусной кислоты, которая используется для чистки и дезинфекции домашних поверхностей.
Яблочная кислота: Эта кислота придает яблокам и другим фруктам свежий и кислый вкус. Она делает их особенно аппетитными и добавляет вкус в различные напитки, соки и кондитерские изделия.
Винная кислота: Эта кислота присутствует в виноградных ягодах и используется в виноделии для придания вину кислого вкуса и активации брожения. Она способствует сохранению свежести и усилению ароматов вина.
Аскорбиновая кислота: Более известная как витамин C, аскорбиновая кислота является одним из самых важных питательных веществ для организма. Она содержится во многих фруктах и овощах, таких как апельсины, киви, зеленый перец и шиповник. Витамин C способствует укреплению иммунной системы и здоровья в целом.
Это только некоторые примеры естественных кислот, которые мы встречаем в нашей повседневной жизни. Они играют важную роль в пищевой промышленности, медицине и других областях. Узнавая о них, мы можем лучше понять, как они влияют на нас и как использовать их в нашу пользу.
Примеры неорганических кислот
Серная кислота (H2SO4)
Соляная кислота (HCl)
Соляная кислота (HCl) — еще одна важная неорганическая кислота. Она широко применяется в промышленности для очистки металлов и производства пластмасс, удобрений и фармацевтических препаратов. Соляная кислота также используется в медицине для борьбы с инфекциями и для более точной регулировки pH в лабораторных и медицинских исследованиях.
Солянокислый аммоний (NH4Cl)
Солянокислый аммоний (NH4Cl) — это соль, производная от соляной кислоты. Она используется в медицине, в производстве лекарств для лечения расстройств желудка. Солянокислый аммоний также используется в лабораторных условиях для регулирования pH и в производстве удобрений.
Фосфорная кислота (H3PO4)
Фосфорная кислота (H3PO4) — это еще одна важная неорганическая кислота. Она используется в промышленности для производства удобрений, пищевых добавок и фосфатных соединений, которые используются для защиты металлов от коррозии. Фосфорная кислота также используется в лаборатории для проведения различных химических реакций и в медицине для лечения некоторых заболеваний и состояний.
Солянокислый натрий (NaCl)
Соль — хороший пример неорганической кислоты. Солянокислый натрий (NaCl) — это один из наиболее распространенных видов соли. Он используется в пищевой промышленности для улучшения вкуса и консервации пищевых продуктов. Солянокислый натрий также используется как противогрибковое средство и для поддержания pH в лабораторных и медицинских исследованиях.
- Серная кислота (H2SO4)
- Соляная кислота (HCl)
- Солянокислый аммоний (NH4Cl)
- Фосфорная кислота (H3PO4)
- Солянокислый натрий (NaCl)
Кислоты в химии: определение и примеры
Кислоты обычно обладают кислотными свойствами, которые включают в себя реакцию с основаниями, образование солей и протолиз. Кислоты могут быть органическими (содержащими углерод) или неорганическими (не содержащими углерод).
Примеры кислот:
- Серная кислота (H2SO4) — это одна из самых распространенных неорганических кислот, используемых в промышленности и лабораториях.
- Уксусная кислота (CH3COOH) — это пример органической кислоты, которая часто используется в пищевой промышленности и бытовых условиях.
- Соляная кислота (HCl) — это также неорганическая кислота, которая широко применяется в лабораторных условиях.
- Формиевая кислота (HCOOH) — это еще одна органическая кислота, которая естественно присутствует в некоторых живых организмах и может использоваться в промышленности.
Это только некоторые примеры кислот, присутствующих в химических реакциях и различных приложениях. Кислоты играют важную роль в химии и на практике и широко используются в различных отраслях промышленности.





