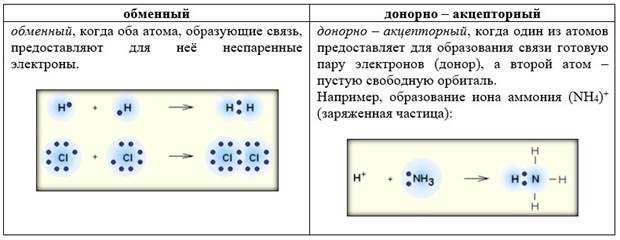
Представь себе молекулу, тесно связанных атомов, которые обладают особой силой, удерживающей их вместе. Эта сила называется ковалентной связью, и она играет важную роль в определении физических и химических свойств соединений.
Однако, ковалентная связь не просто случайное слияние атомов. Она обладает определенной направленностью, что означает, что каждый атом внутри молекулы ориентирован в определенном направлении. Эта особенность определяется принципами, которым подчиняется ковалентная связь.
Давай разберемся подробнее, что такое направленность ковалентной связи и какие принципы лежат в ее основе.
Связь в химии
В целом, химическая связь – это энергетическое явление, которое возникает между атомами, ионами или молекулами и обусловливает их структуру и свойства. Она основана на обмене или совместном использовании электронов. Атомы или молекулы схлопываются вместе, чтобы достичь наиболее устойчивого состояния и образовать соединения.
Теперь, давайте представим себе атомы как маленькие строительные блоки, а связь – это клей, который держит их вместе. Только вместо обычного клея используется энергия. Связь в химии – это не просто скрепляющий элемент, она определяет форму и структуру соединения. Как и в случае с клеем, связь может быть крепкой или слабой, в зависимости от типа связи и взаимодействия между атомами.
Важно отметить, что химическая связь имеет направленность. Это означает, что электроны, участвующие в связи, распределены между атомами или молекулами не симметрично. Они проводят больше времени вблизи одного из атомов, создавая неравномерное распределение зарядов и образуя полярную или ионную связь.
Интересно, не правда ли? Мы уже знаем, что связь в химии обеспечивает структуру и свойства вещества, а также влияет на взаимодействие с другими веществами. Теперь давайте ответим на вопрос: зачем это все нам нужно?
Представьте, что вы химик-исследователь. Вы хотите создать новое вещество, которое могло бы помочь в разработке лекарства, новых материалов или энергетических источников. Вам необходимо понять, какие атомы нужно соединить и каким образом, чтобы получить нужный продукт. Именно знание о химической связи позволяет химикам превращать простые элементы в сложные соединения, которые могут иметь огромное значение для нашей жизни.
Так что химическая связь – это ключевой фактор в понимании и изучении мира химии. Без нее не было бы химических реакций, соединений и всех явлений, которые связаны с химией. Она позволяет нам разрабатывать новые технологии, создавать новые материалы и находить решения для глобальных проблем. Поэтому погрузитесь в мир химических связей, и вы обнаружите, что он полон удивительных открытий и возможностей!
Ковалентная связь
Здравствуйте! Сегодня я хочу рассказать вам о ковалентной связи, одной из фундаментальных концепций в химии. Итак, давайте начнем!
Ковалентная связь — это особый тип химической связи, которая образуется между атомами при совместном использовании их внешних электронов. Грубо говоря, это связь, в которой атомы «делят» свои электроны, чтобы достичь полностью заполненной внешней оболочки. В результате, образуется пара электронов, называемых электронной парой, которая ковалентно связывает два атома.
Основные принципы ковалентной связи заключаются в следующем:
- Совместное использование электронов. В ковалентной связи атомы обмениваются электронами таким образом, чтобы установить электронную пару между ними. Это происходит часто с атомами неметаллов.
- Образование молекул. Ковалентная связь позволяет объединять атомы в молекулы. Молекулы могут содержать как два атома, так и более.
- Образование новых энергетических состояний. Ковалентная связь образует устойчивые структуры, в которых энергия системы становится минимальной. Это позволяет образовывать различные химические соединения.
Ковалентная связь является основой многих химических реакций и процессов в природе. Она позволяет создавать разнообразные вещества, от простых органических соединений до сложных полимерных материалов. Без ковалентной связи наш мир был бы невозможен!
Теперь давайте представим, как бы выглядел наш мир без ковалентной связи. Не было бы многообразия органических соединений, которые образуют основу жизни на Земле. Мы бы не имели полимерных материалов, таких как пластик, которые широко используются в нашей повседневной жизни. Все химические процессы и реакции в организмах были бы невозможны без ковалентной связи.
Итак, ковалентная связь — это не только основа химии, но и ключевой компонент жизни на Земле. Благодаря ковалентной связи мы можем исследовать ее удивительные свойства и применять их в различных областях науки и технологий. Будьте любопытными и исследуйте мир ковалентной связи!
Суть ковалентной связи
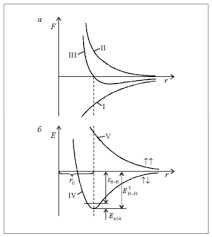
Очень удобно представить ковалентную связь как своеобразный танец двух атомов, в котором они дарят и получают электроны друг у друга. Представь себе, как два лучших друзья танцуют румбу. Они так синхронизированы, что танцуют в полном соответствии друг с другом. Именно так происходит и в случае ковалентной связи: атомы делят электроны между собой так, что они двигаются в гармонии и равновесии.
В ковалентной связи электроны могут быть общими для двух атомов или могут принадлежать только одному атому, но совместно использоваться для связи. Это создает более сложную систему, которая обеспечивает стабильность и устойчивость молекулы. И несмотря на то, что ковалентная связь может быть очень сильной, некоторые атомы предпочитают образовывать более одной связи, чтобы достигнуть идеального равновесия.
Зачастую, чтобы лучше понять суть ковалентной связи, полезно посмотреть на примеры из повседневной жизни. Например, вода – это молекула, состоящая из двух атомов водорода и одного атома кислорода. В процессе образования воды атомы водорода и кислорода делят пару электронов, чтобы они могли двигаться вместе, создавая структуру воды. Из-за этой структуры, вода обладает уникальными свойствами, такими как высокая теплопроводность и способность растворять множество веществ.
Так что, дорогой читатель, ковалентная связь – это не просто взаимодействие атомов, а настоящее творчество, в результате которого появляются новые вещества с уникальными свойствами. Это как вечер на танцполе, когда два атома танцуют в гармонии и создают потрясающее представление, которое мы называем ковалентной связью.
Принципы направленности ковалентной связи
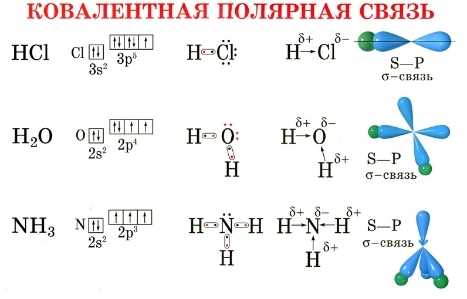
Первый принцип направленности ковалентной связи — геометрическая форма молекулы. Когда атомы образуют ковалентную связь, они стараются занять такое пространственное положение, при котором энергия системы будет минимальной. Это приводит к определенной форме молекулы, которая зависит от типа связи и числа электронных пар.
Например, в молекуле воды, кислородный атом центральный и формирует две ковалентные связи с двумя водородными атомами. Это приводит к формированию угла между связями водород-кислород, который составляет примерно 104.5 градусов. Такая геометрическая форма обусловлена стремлением молекулы к минимальной энергии.
Второй принцип направленности ковалентной связи – симметрия. Связь обладает направлением, которое может быть представлено стрелкой, указывающей на район, где находится пара атомов. Это позволяет предсказывать форму молекулы и ее свойства.
Например, в случае молекулы аммиака, один азотный атом образует трехцентровую ковалентную связь с тремя водородными атомами. Форма молекулы аммиака определяется симметрией этой связи, а именно направлением пары электронов в пространстве.
Третий принцип направленности ковалентной связи – длина связи. Длина ковалентной связи является важным параметром, который определяется типом и степенью связи между атомами. Ковалентная связь может быть одинарной, двойной или тройной в зависимости от количества электронных пар, которыми они делятся.
Например, в молекуле метана, каждый из четырех водородных атомов образует одинарную ковалентную связь с центральным атомом углерода. Длина связи в этой молекуле зависит от радиусов атомов и составляет около 109 пикометров.
Итак, принципы направленности ковалентной связи включают геометрическую форму молекулы, симметрию связи и длину связи. Понимание этих принципов позволяет нам лучше понять структуру молекул и их свойства, а также применять этот знания в различных областях науки и промышленности.
Влияние направленности ковалентной связи
Основное влияние направленности ковалентной связи заключается в так называемой «организованности» структуры вещества и его реакционной способности. Направленность ковалентной связи может определять форму молекулы, а также внутримолекулярные взаимодействия и свойства соединения.
Например, вода — это простое вещество, состоящее из атомов водорода и кислорода, связанных ковалентными связями. Благодаря направленности этих связей, молекулы воды образуют угол, который придает ей особую форму. Кроме того, направленность ковалентной связи в воде способствует образованию водородных связей, которые делают вещество устойчивым и позволяют проявляться его уникальным свойствам — высокой температуре кипения, теплоемкости и способности растворять множество веществ.
Направленность ковалентной связи также влияет на химическую активность и реакционную способность вещества. Так, например, волокна растений и животных состоят из органических соединений, связанных ковалентными связями. Благодаря ориентации этих связей, волокна обладают уникальными свойствами прочности и гибкости, позволяющими им исполнять свои функции в организмах.
Важно отметить, что направленность ковалентной связи является результатом взаимодействия различных факторов, включая электронную структуру атома, его электроотрицательность и геометрию. Исследование и понимание этих факторов позволяет нам лучше понять и контролировать свойства вещества.
Направленность ковалентной связи: суть и принципы
Принципы направленности ковалентной связи определяются геометрией орбиталей и положением ядер атомов. Главными принципами являются:
- Геометрия орбиталей – орбитали, участвующие в образовании ковалентной связи, имеют определенную форму – шаровидную, плоскую или сильно вытянутую. Таким образом, молекулы приобретают определенную топологию, что влияет на их реакционную способность и физические свойства.
- Положение ядер атомов – расположение ядер атомов в молекуле влияет на направленность ковалентной связи. Если атомы находятся на одной линии, связь будет линейной. В случае, когда атомы формируют угол, связь будет угловой. Это обусловлено взаимодействием между электронными облаками и ядрами атомов.
- Взаимное влияние атомов – ковалентная связь возникает из-за взаимного влияния атомов, анализируется знаком силы реальных, отталкивающих частот и силы энергии. В случае положительного вклада взаимодействие будет на пользу образованию связи, а в случае отрицательного – на разрыв связи.
Таким образом, направленность ковалентной связи – важное свойство, которое определяет структуру молекул и их химические свойства. Она зависит от геометрии орбиталей, положения ядер атомов и взаимного влияния атомов.




