В химии, основания — это вещества, которые могут принимать водородные ионы (протоны) и образовывать ионы гидроксида. Они обладают щелочными свойствами и могут растворяться в воде, образуя щелочные растворы.
Одним из примеров основания является щелочь — сильное основание, которое образует ионы гидроксида (OH-) при растворении в воде. Калий и натрий являются основными компонентами многих щелочей, таких как гидроксид калия (KOH) и гидроксид натрия (NaOH), которые широко используются в индустрии и бытовых нуждах.
Основания играют важную роль в реакциях в химии и имеют множество приложений в различных отраслях науки и промышленности.
Определение оснований
Основания обладают несколькими основными характеристиками:
- Способность принимать протоны: основания имеют свободные пары электронов, которые могут принять протоны от кислоты.
- Образование гидроксида: при реакции с водой основания образуют гидроксиды.
- Высокий pH: основания обладают высоким pH, это значит, что они могут уменьшать концентрацию водородных ионов в растворе и делать его менее кислым.
Основания можно классифицировать на несколько типов:
- Органические основания: это основания, содержащие атомы азота или других элементов в своей структуре. Некоторые примеры органических оснований включают аммиак (NH3) и аминокислоты.
- Неорганические основания: это основания, не содержащие атомы углерода. Наиболее известным примером является гидроксид натрия (NaOH).
Основания играют важную роль в различных областях, включая химическую промышленность, медицину, сельское хозяйство и домашнюю химию. Например, они используются в процессе нейтрализации кислот, чтобы избавиться от их вредных эффектов или в качестве веществ для очистки воды. Основания также широко применяются в лекарствах и косметике.
Таким образом, основания — неотъемлемая часть химии, которая играет важную роль во многих сферах нашей жизни. Они позволяют нам решать ряд проблем и улучшать качество жизни. Знание оснований и их свойств является ключевым для понимания многих химических процессов и их применений.
Химические свойства оснований
Одно из основных химических свойств оснований — способность принимать протоны (H+) и образовывать ионы гидроксида (OH-). Это происходит в результате реакции основания с водой, которая называется гидролизом. Гидролизные реакции оснований могут быть экзотермическими или эндотермическими.
Некоторые основания могут образовывать растворы сильных щелочей, таких как гидроксид натрия (NaOH) и гидроксид калия (KOH). Эти вещества имеют высокую щелочность и активно реагируют с кислотами, образуя соль и воду.
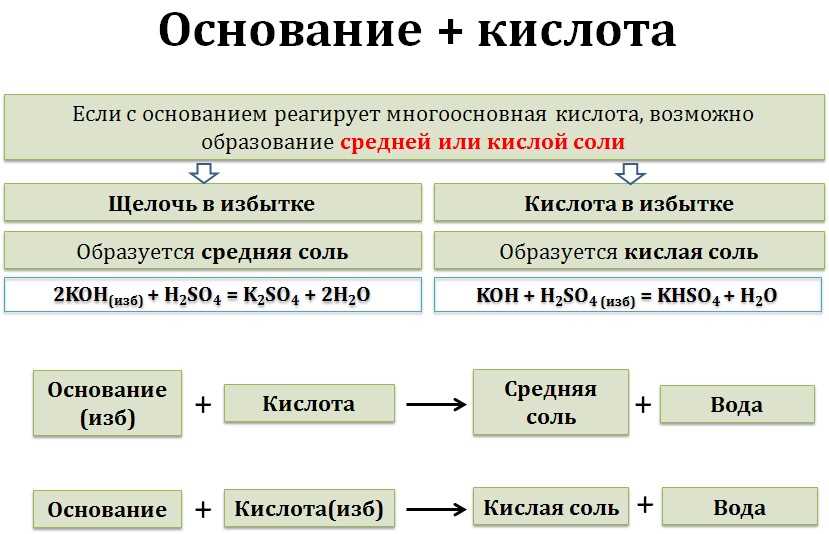
Еще одно интересное химическое свойство оснований — их способность нейтрализовать кислоты. Когда растворы оснований смешиваются с растворами кислот, происходит реакция нейтрализации, в результате которой образуются соль и вода. Это свойство оснований является основой для процессов нейтрализации, которые широко используются в химической промышленности и в повседневной жизни.
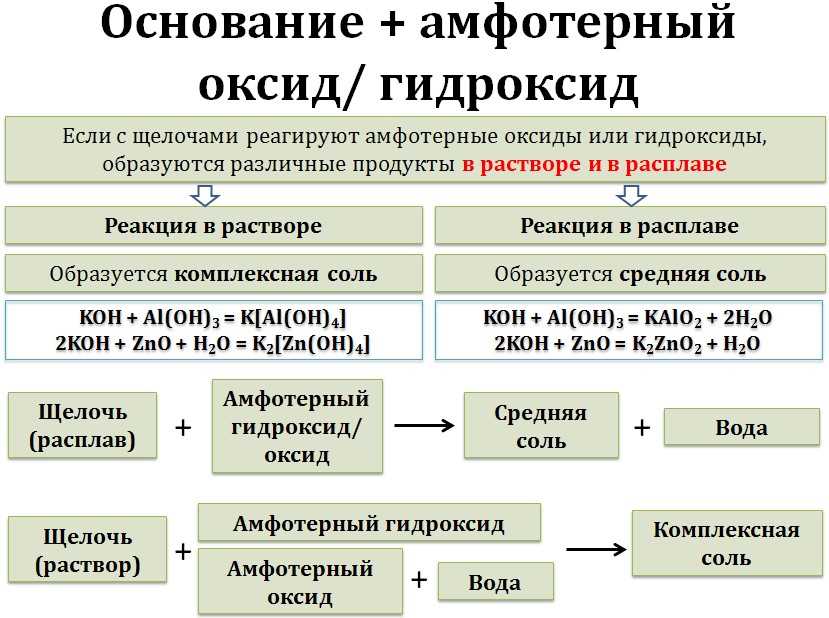
Основания также могут обладать амфотерными свойствами, что означает, что они могут и как кислота, и как основание реагировать с другими веществами. Это делает их универсальными реагентами и позволяет им участвовать в различных химических реакциях и процессах.
Химические свойства оснований важны для понимания их реактивности и их роли во многих процессах, включая нейтрализацию, гидролиз и образование солей. Знание этих свойств помогает химикам и научным исследователям использовать основания в различных областях, включая медицину, сельское хозяйство и производство.
- Способность принимать протоны и образовывать ионы гидроксида.
- Способность образовывать растворы сильных щелочей.
- Способность нейтрализовать кислоты.
- Амфотерные свойства — способность реагировать как кислота, так и основание.
Видите ли вы, как важны основания в химии? С их уникальными химическими свойствами, они играют центральную роль во многих процессах и реакциях. Они могут быть щелочными, нейтрализующими, амфотерными — основания всегда готовы к взаимодействию. Подумайте о том, как вы можете применить знание об этих свойствах в повседневной жизни или даже в химических экспериментах. Мир химии ждет ваших открытий!
Примеры оснований
1. Гидроксид натрия (NaOH)
Гидроксид натрия, или щелочь, является одним из наиболее распространенных оснований. Оно широко используется в различных областях, включая бытовую химию и производство пищевых продуктов. Например, его можно найти в моющих средствах, средствах для разжижения красок и консервантах для пищи.
2. Гидроксид калия (KOH)
Гидроксид калия — еще одно основание, часто используемое в производстве. Оно широко применяется в производстве мыла, бумаги и стекла. Также гидроксид калия может использоваться как растворитель для удаления грязи и жира.
3. Аммиак (NH3)
Аммиак – это газообразное основание, которое широко используется в производстве удобрений, а также в бытовой сфере. Он может быть присутствовать в многих бытовых чистящих средствах и обеспечивать их щелочную среду для эффективного удаления грязи.
4. Кальций гидроксид (Ca(OH)2)
Кальций гидроксид, также известный как пустотелый известняк, используется в различных сферах, включая строительство и сельское хозяйство. Он применяется как нейтрализатор кислотности почвы, а также в производстве строительных материалов, таких как известь.



