Разбираясь с фундаментальными элементами нашей вселенной, мы не можем обойти вниманием основное состояние атома и его особенности. Атомы, как строительные блоки вещества, являются основной формой существования материи. Их структура и свойства определяют все процессы, происходящие в природе и в нашей жизни.
Узнавая о составе и поведении атомов, мы погружаемся в мир частиц и энергии, понимая, что все вокруг нас– результат взаимодействия атомных структур. Развитие науки и современные технологии позволяют нам взглянуть глубже в тайны атомной природы и использовать эти знания во благо человечества.
В этой статье мы рассмотрим основные свойства атома и его роль в мире вещества. Готовы окунуться в удивительный мир микромира атомов?
Химическая структура атома
Атом — это фундаментальная частица, из которой состоят все вещества в нашей вселенной. Каждый атом состоит из трех основных компонентов: электронов, протонов и нейтронов. Электроны — это негативно заряженные частицы, которые вращаются вокруг ядра атома. Протоны — это положительно заряженные частицы, которые находятся в ядре атома. Нейтроны — это нейтральные по заряду частицы, которые также находятся в ядре вместе с протонами.
Химическая структура атома определяется числом электронов, протонов и нейтронов. Количество протонов в атоме определяет его атомный номер и определяет его элемент в периодической системе. Количество нейтронов может варьироваться, что приводит к образованию изотопов одного и того же элемента. А количество электронов определяет электронную конфигурацию атома, его химические свойства и способность взаимодействовать с другими атомами.
Интересно то, что электроны в атоме располагаются на разных энергетических уровнях или оболочках. Наиболее близки к ядру находится первая оболочка, которая может содержать не более 2 электронов. Вторая оболочка может содержать до 8 электронов, а третья — до 18. Каждая оболочка заполняется электронами в соответствии с определенными правилами, которые определяют его химические свойства и реактивность.
Цель научного изучения химической структуры атома заключается в понимании, как атомы и их компоненты взаимодействуют друг с другом. Понимая эти взаимодействия, мы можем создавать новые вещества, улучшать существующие и разрабатывать новые технологии.
Вся эта сложная система химической структуры атома — это своего рода паззл, и мы только начинаем понимать его глубины. Но я верю, что наш увлекательный путь разгадки химической структуры атома приведет нас к новым открытиям и прогрессу, который будет полезен и интересен для всех нас.
Основные свойства атома
1. Масса атома
Масса атома определяется протонами и нейтронами, находящимися в ядре. Протоны имеют положительный заряд, а нейтроны не имеют заряда. Каждый протон и нейтрон имеет примерно одинаковую массу, которая составляет примерно 1 атомную единицу массы (ат.м.е.). Масса электронов крайне мала по сравнению с массой протонов и нейтронов и практически не учитывается при расчетах общей массы атома.
2. Заряд атома
Заряд атома определяется количеством протонов и электронов. Протоны имеют положительный заряд, а электроны — отрицательный. Если число протонов равно числу электронов, то атом будет нейтральным, без электрического заряда. Если количество электронов меньше количества протонов, то атом будет иметь положительный заряд, и наоборот, если количество электронов больше количества протонов, атом будет иметь отрицательный заряд.
3. Размер атома
Атомы имеют очень маленький размер. Радиус атома варьирует от нескольких пикометров (1 пикометр = 1 триллионная доля метра) до нескольких ангстремов (1 ангстрем = 0,1 нанометра). Несмотря на свой маленький размер, атомы являются основными строительными блоками всего, что существует в материальном мире.
4. Изотопы
Атомы одного и того же элемента могут иметь разное количество нейтронов в своих ядрах. Эти варианты атомов называются изотопами. Изотопы имеют одинаковое количество протонов и разное количество нейтронов. Некоторые изотопы могут быть нестабильными и распадаться со временем, испуская радиацию.
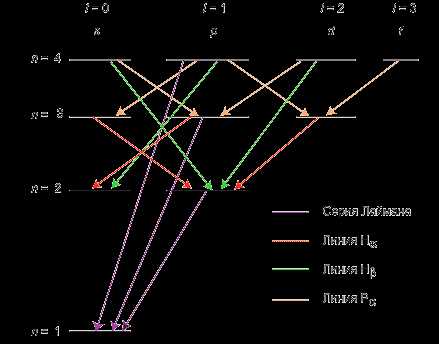
5. Энергетические уровни
Электроны в атоме находятся на определенных энергетических уровнях. Каждый энергетический уровень представляет различную энергию электрона. Возможность электронов передвигаться между энергетическими уровнями и поглощать или испускать энергию позволяет атомам обладать химической активностью и образовывать химические связи.
6. Ядерные реакции
Ядро атома может претерпевать ядерные реакции, такие как деление или слияние. При делении ядер атома освобождается большое количество энергии, которая может использоваться в ядерной энергетике. Слияние ядер приводит к образованию новых элементов и является процессом, который происходит в звездах.
7. Электромагнитные взаимодействия
Атомы могут взаимодействовать друг с другом путем обмена или передачи электронов. Эти электромагнитные взаимодействия отражаются в свойствах химических соединений и молекул. Они определяют химическую реакцию, способность вещества образовывать связи с другими веществами и его поведение в различных условиях.
Все эти свойства атома являются основой для понимания его роли в химических и физических процессах. Изучение этих свойств позволяет нам лучше понять мир вокруг нас и создавать новые материалы и технологии для улучшения нашей жизни. Какие из этих свойств атома вас больше всего удивляют либо мотивируют исследовать дальше? Поделитесь своими мыслями и вопросами в комментариях!
Внутренняя энергия атома
Когда атом находится в равновесии, его внутренняя энергия достигает минимума. Однако, поскольку на атомы оказывают влияние различные силы, эта энергия может изменяться. Например, при нагревании атомы начинают двигаться более активно, что приводит к увеличению их внутренней энергии.
Внутренняя энергия атома играет важную роль в различных физических процессах. Она определяет температуру вещества, его состояние (твердое, жидкое или газообразное) и способность взаимодействовать с другими атомами. Кроме того, внутренняя энергия влияет на химические реакции и может быть использована для получения электроэнергии в ядерных реакторах.
Понимание внутренней энергии атома позволяет нам лучше понять природу материи и использовать ее в нашу пользу. Например, благодаря пониманию принципов работы атомного реактора, мы можем производить чистую электроэнергию. Кроме того, исследование внутренней энергии атома открывает нам новые возможности в областях физики, химии и материаловедения.
Основное состояние атома: сущность и свойства

Основное состояние атома характеризуется следующими свойствами:
- Энергетический уровень: В основном состоянии атом находится на наименьшем энергетическом уровне. Это состояние соответствует энергии, которую атом получает при образовании связи с другими атомами или молекулами.
- Распределение электронов: В основном состоянии атом имеет определенное число электронов. Распределение электронов вокруг ядра атома определяет его электронную конфигурацию и его химические свойства.
- Размер атома: В основном состоянии атом имеет определенный размер, который зависит от его ядерного заряда и электронной оболочки. Размер атома определяет его физические свойства, такие как плотность и объем.
- Химические свойства: Основное состояние атома определяет его химические свойства. Они включают его возможность образования связей с другими атомами или молекулами, его реактивность и активность.
Основное состояние атома является исходным состоянием, от которого могут происходить изменения под воздействием различных факторов, таких как температура, давление или внешние реагенты. Знание и понимание основного состояния атома позволяет установить его характеристики и использовать их для разработки новых материалов и технологий.





