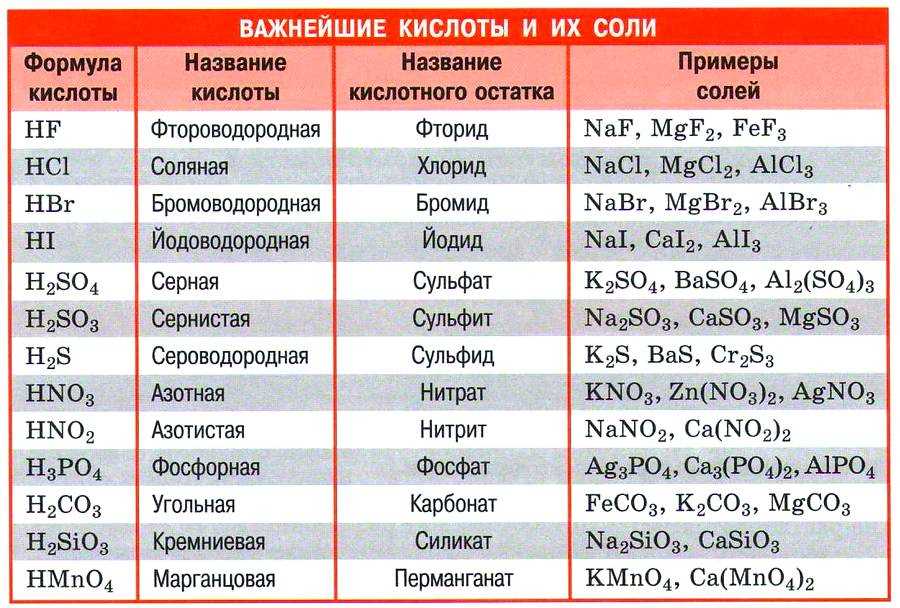
Кислоты – это важные химические соединения, которые играют ключевую роль во многих сферах нашей жизни. Они обладают определенными свойствами, благодаря которым находят применение в различных областях, включая науку, медицину, производство и пищевую промышленность. Основные кислоты, такие как серная, соляная и азотная, являются ключевыми компонентами многих веществ и материалов. Они могут быть использованы в качестве катализаторов, реагентов, антиоксидантов и многого другого. Понимание свойств и применение основных кислот являются важным аспектом как для профессионалов, так и для широкой публики.
- Что такое кислоты
- Определение кислот
- Свойства кислот
- Различные виды кислот
- Органические кислоты
- Неорганические кислоты
- Аминокислоты
- Аскорбиновая кислота
- Фосфорная кислота
- Уксусная кислота
- Свойства кислот
- Кислотность и щелочность
- Кислотные реакции
- Физические свойства кислот
- Основные кислоты: понятие, свойства и применение
- Свойства основных кислот:
- Применение основных кислот:
- Примеры основных кислот:
Что такое кислоты
Ведь многие из нас уже слышали о таких известных кислотах, как уксусная кислота или соляная кислота. Но это только малая часть всего кислотного мира. И кислоты бывают разные, каждая со своими уникальными свойствами и применением.
В химии кислоты — это вещества, которые обладают кислотными свойствами. Их общей характеристикой является то, что они способны отдавать отрицательно заряженные водородные ионы или протоны при взаимодействии с водой.
- Когда мы говорим о протонной или классической кислоте, мы обычно имеем в виду водные растворы кислотных соединений, в которых протоны существуют в виде водородных ионов.
- Также существуют и другие типы кислот, такие как карбоксильные кислоты, которые содержат карбоксильные группы COOH, и сульфоновые кислоты, содержащие сульфонильную группу SO3H.
Кислоты могут быть как органическими, то есть содержать углерод, так и неорганическими, не содержащими углерода. Они могут существовать в жидком или твердом состоянии, и даже в газообразной форме, как, например, хлороводородная кислота.
Теперь мы можем задаться вопросом: для чего все-таки используются эти кислоты? Почему мы должны знать о них?
Ответ прост: кислоты играют важную роль во многих областях жизни, начиная от химической промышленности и заканчивая медициной и пищевой промышленностью.
Они используются в процессе производства различных продуктов, включая лекарства, удобрения, пищевые добавки, косметические продукты и многое другое.
Органические кислоты, такие как лимонная, молочная или уксусная, используются в кулинарии для придания вкуса и консервации продуктов.
Неорганические кислоты, такие как серная или соляная, находят применение в процессе очистки воды, исправления рН-баланса почвы, а также в химической аналитике и лабораторных исследованиях.
Кислоты также являются ключевыми активными компонентами в различных косметических и уходовых средствах, таких как шампуни или пилинги.
В медицине кислоты используются для производства лекарств и медицинских средств, используемых для лечения различных заболеваний.
В общем, кислоты являются неотъемлемой частью нашей жизни и нашей окружающей среды. Их высокая активность и широкое применение делают их важными компонентами в различных областях нашей деятельности.
Всегда интересно узнавать больше о мирах, которые нас окружают. И хотя мы не всегда задумываемся об их существовании, знание о кислотах помогает нам лучше понять и оценить важность этих удивительных веществ в нашей повседневной жизни.
Определение кислот
Кислоты — это вещества, которые имеют способность отдавать протоны (водородные ионы) в растворе. Они состоят из атомов, объединенных в молекулы. У этих молекул есть особенные атомы — кислород и водород, которые играют важную роль в химических реакциях.
Вы, наверное, сталкивались с кислотами в повседневной жизни. Какие кислоты мы обычно используем? Например, лимонная кислота, которая придает лимонам свой характерный вкус. Или уксусная кислота, которую используют в кулинарии и для уборки. Еще одна известная кислота — соляная кислота, используемая в промышленности и научных исследованиях.
Кислоты могут быть разных видов, в зависимости от количества протонов, которые они могут отдать. Некоторые кислоты могут отдать только один протон, они называются моноосновными кислотами. Другие кислоты могут отдать два или более протонов, они называются полиосновными кислотами.
Кислоты могут быть органическими и неорганическими. Органические кислоты, такие как лимонная кислота и уксусная кислота, содержат углеродные атомы в своей структуре. Неорганические кислоты, такие как соляная кислота и серная кислота, не содержат углерод и в основном получаются из минералов.
Важно помнить, что кислоты могут быть как сильными, так и слабыми. Сильная кислота способна отдать протон полностью в растворе, в то время как слабая кислота может отдать только часть протонов.
Теперь вы знаете основное определение кислот и несколько примеров их использования. У вас есть опыт взаимодействия с кислотами в повседневной жизни или в своей работе? Расскажите о нем в комментариях!
Свойства кислот
1. Кислотность
Одно из ключевых свойств кислот – это их кислотность. Кислотность – способность кислоты отдавать водородные ионы (H+). Чем больше водородных ионов отдает кислота, тем сильнее ее кислотность. Кислотность можно измерять с помощью pH-метра, который указывает на кислотность или щелочность раствора.
Например, лимонный сок и уксус считаются кислыми, так как они обладают высокой кислотностью и имеют низкий pH-уровень.
2. Кислотные реакции
Кислоты обладают способностью вступать в реакции с другими веществами. Кислотная реакция может проявляться в разных формах, таких как образование солей, выделение газа или изменение окраски раствора.
Например, реакция хлороводородной кислоты (HCl) с гидроксидом натрия (NaOH) приводит к образованию соли натрия (NaCl) и воды (H2O).
3. Коррозивность
Одно из негативных свойств некоторых кислот – их коррозивность. Кислоты могут вызывать разрушение или повреждение материалов, таких как металлы и ткани. Это связано с их способностью реагировать с металлическими ионами и вызывать окисление или образование солей.
Например, серная кислота (H2SO4) может вызвать коррозию металлических поверхностей.
4. Применение
Кислоты имеют широкий спектр применений в разных отраслях. Например, соляная кислота (HCl) используется в производстве пластиков и удобрений, серная кислота (H2SO4) – в аккумуляторах и производстве удобрений, а уксусная кислота (CH3COOH) – в кулинарии.
Какие кислоты вы уже встречали в повседневной жизни?
В целом, свойства кислот определяют их важность и значимость в химических процессах и промышленности. Понимание этих свойств помогает использовать их с умом и вниманием к окружающей среде.
Различные виды кислот
Органические кислоты
Одним из наиболее распространенных видов кислот являются органические кислоты. Они содержат углеродные атомы в своей структуре и играют важную роль в биологических процессах. Например, яблочная кислота, которая присутствует в различных фруктах, придает им кислый вкус. Молочная кислота образуется в мышцах во время физической активности и может вызвать ощущение усталости.
Неорганические кислоты
Неорганические кислоты, в отличие от органических, не содержат углерод. Они широко используются в промышленности и находятся в различных химических продуктах. Серная кислота, например, используется в производстве удобрений, пластиков и красителей. Хлороводородная кислота используется в лабораторной работе и в производстве химических соединений.
Аминокислоты
Аминокислоты являются основными строительными блоками белков, которые необходимы для нашего организма. Они играют ключевую роль в образовании новых тканей, ремонте поврежденных клеток и поддержании функций органов. Примеры аминокислот включают глутамин, который помогает укрепить иммунную систему, и лейцин, который способствует росту мышц.
Аскорбиновая кислота
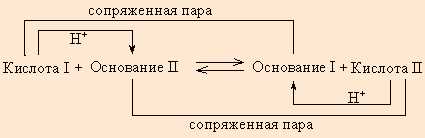
Аскорбиновая кислота, или витамин C, является одной из самых известных кислот. Она играет важную роль в поддержании нашего иммунитета, укреплении здоровья кожи и улучшении поглощения железа. Витамин C можно найти во многих фруктах и овощах, таких как цитрусовые, киви и красный перец.
Фосфорная кислота
Фосфорная кислота — еще одна важная кислота, которая играет роль в многих биологических и химических процессах. Она участвует в образовании ДНК и РНК, энергетическом обмене в организме и регулировании кислотно-щелочного баланса. Кроме того, фосфорная кислота используется в производстве удобрений и стиральных средств.
Уксусная кислота
Уксусная кислота, которую мы используем в кулинарии в виде уксуса, также имеет много других применений. Она используется в производстве пищевых добавок, уксусной эссенции, ацетона и различных растворителей. Уксусная кислота также может использоваться как очиститель и антисептик в бытовых условиях.
- Органические кислоты — содержат углеродные атомы и играют важную роль в биологических процессах.
- Неорганические кислоты — не содержат углерод и широко используются в промышленности.
- Аминокислоты — основные составляющие белков, необходимые для нашего организма.
- Аскорбиновая кислота — также известна как витамин C, играет важную роль в поддержании здоровья.
- Фосфорная кислота — участвует в биологических и химических процессах.
- Уксусная кислота — широко используется в пищевой промышленности и домашнем хозяйстве.
Свойства кислот
Первое свойство кислот, о котором я хочу рассказать, — это их способность реагировать с щелочами и образовывать с ними соли. Это свойство называется кислотностью. Знакомая нам лимонная кислота, например, является кислотной соединением и отличается кислотностью.
Еще одно важное свойство кислот — их способность вызывать раздражение или ожоги при попадании на кожу или слизистые оболочки. Поэтому кислоты обычно хранятся и транспортируются с особыми мерами предосторожности. Но не переживайте, у нас же есть защитная одежда и особые меры безопасности, чтобы обрабатывать и использовать кислоты безопасно.
Еще одно интересное свойство кислот — это их способность менять цвета некоторых органических соединений. Например, хлороводородная кислота может изменить цвет индикатора из синего в красный.
Итак, кислоты — это удивительные соединения, которые имеют множество интересных свойств. Они помогают нам в жизни, используются в наших бытовых и промышленных нуждах, и несомненно являются важной частью нашего мира.
Кислотность и щелочность
Здравствуйте! Сегодня я хотел бы рассказать вам о кислотности и щелочности, двух основных свойствах веществ, с которыми мы сталкиваемся в повседневной жизни. Вы знаете, что жидкости и различные химические соединения могут быть либо кислотными, либо щелочными, а может быть и нейтральными. А как вы связываете эти свойства с вашими ежедневными делами?
Представьте: вы с друзьями планируете приготовить вкусный обед по рецепту вашей бабушки. Вы берете в руки лимон, чувствуете кислинку на языке и сразу понимаете, что это кислотное вещество. На столе лежат мыло и подгузники — вы знаете, что мыло щелочное, а подгузники — нейтральные. И вот вы, вектормицыки планируете сделать котлеты из фарша — вы их тщательно ожидаете лимонным соком, что делает фарш мягким и сочным. А когда вы помываете посуду после обеда, мылом, вы знаете, что в нем содержится щелочь, которая помогает очистить поверхности от жира и бактерий. Удавутие так просто использовать обычные химические свойства веществ, чтобы создать лучшие блюда и обеспечить гигиену вашего дома!
Но давайте теперь обратимся к научным терминам. Кислотность и щелочность определяются величиной pH, которая указывает на уровень концентрации ионов водорода в растворе. pH-значения меньше 7 обозначают кислотные вещества, а значения больше 7 — щелочные. Таким образом, нейтральные вещества имеют pH около 7.
Какие свойства имеют кислотные и щелочные вещества? Кислоты обычно имеют острый запах, они коррозивны (могут разъедать прочные материалы) и причинять жжение на коже или слизистых оболочках. Некоторые кислоты, такие как соляная кислота, используются в промышленности для очистки и дезинфекции. Щелочи, например, натрий гидроксид, обладают горьким вкусом и ощущением жжения. Они также используются в различных областях, включая производство мыла и моющих средств.
Захотите-ли вы научиться определять кислотность или щелочность вещества без pH-метра или специальных индикаторов? Моя сестра, например, начала изучать экологию и биологию, и ей пришлось проводить много опытов с растворами. Однажды она показала мне, как она определяет кислотность раствора с помощью капельки сока красного капусты. Когда капелька попадает в кислотный раствор, он становится красным, а в щелочном — зеленым. Вот таким способом можно сделать науку более доступной и веселой!
Кислотные реакции
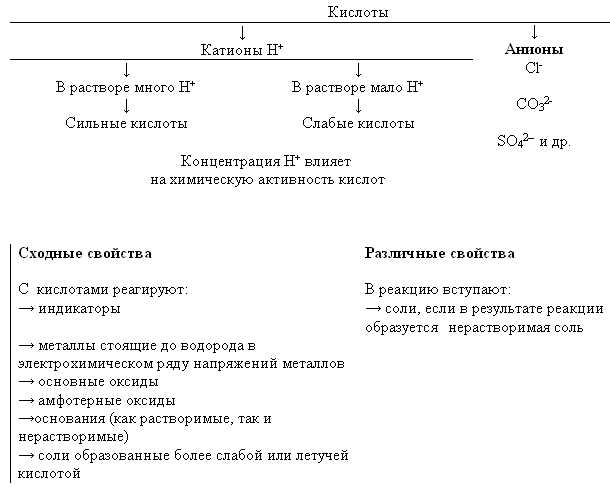
Один из наиболее распространенных примеров кислотной реакции — образование соли. Когда кислота реагирует с щелочью, они образуют соль и воду. Это называется нейтрализационной реакцией. Например, реакция между серной кислотой (H2SO4) и натрий гидроксидом (NaOH) приводит к образованию соли натрия (Na2SO4) и воды (H2O).
Кислотные реакции также могут протекать с участием металлов. Например, когда железо (Fe) реагирует с соляной кислотой (HCl), образуется соль железа (FeCl2) и водород (H2). Это называется реакцией активного металла с кислотой.
Кроме того, кислотные реакции могут происходить с органическими соединениями. Например, уксусная кислота (CH3COOH) может реагировать с этиловым спиртом (C2H5OH) для образования этилового ацетата (C4H8O2) и воды.
Кислотные реакции широко применяются в химической промышленности, медицине, пищевой промышленности и других областях. Например, кислоты используются для производства удобрений, пищевых добавок, лекарств и других продуктов. Они также используются для очистки воды, выведения изделий из железа и др.
Важно помнить, что кислоты имеют различные уровни кислотности и их реактивность зависит от их концентрации и химической структуры. Кроме того, необходимо соблюдать осторожность при работе с кислотами, поскольку они могут быть едкими и опасными для здоровья.
Физические свойства кислот
Одно из наиболее известных физических свойств кислот – их кислотность. Это способность кислоты давать ион водорода (H+) при растворении в воде. Насколько кисла данная субстанция может быть, можно оценить по значениям pH, показывающим концентрацию ионов водорода в растворе. Чем меньше значение pH, тем более кисла считается жидкость или раствор. Например, уксусная кислота обладает низким pH и поэтому классифицируется как кислая субстанция. Благодаря своей кислотности, кислоты активно взаимодействуют с другими веществами.
Другое важное физическое свойство кислот – их состояние в обычных условиях. Некоторые кислоты существуют в виде газов, таких как хлороводородная кислота или сероводородная кислота. Они имеют острый запах и обычно используются в промышленности. Тем не менее, большинство кислот являются жидкими веществами при комнатной температуре, например, серная кислота или азотная кислота. Они обладают впечатляющей густотой и служат для различных технических целей.
Также имеются кислоты, которые могут существовать в виде кристаллической структуры, такие как соляная кислота. Прозрачные и хрупкие кристаллы соляной кислоты используются в медицине, лабораторных исследованиях и других областях. Их физические свойства, такие как точка плавления и плотность, определяются молекулярной структурой и родом связей между атомами вещества.
Кроме того, кислоты могут проявлять различные свойства при воздействии на окружающую среду. Некоторые кислоты обладают высокими температурами кипения и возгоняются при нагревании. Другие кислоты обладают электропроводностью и могут использоваться в электролитах или аккумуляторах. Также существуют кислоты, которые могут выступать в роли окислителей, способных окислять другие вещества и изменять их состав.
Основные кислоты: понятие, свойства и применение
Основными кислотами являются минеральные и органические кислоты. Минеральные кислоты получают из минеральных солей или из продуктов промышленного производства. Органические кислоты содержатся в растениях и животных организмах.
Свойства основных кислот:
- Кислотные вкусы: Основные кислоты имеют кислый вкус.
- Растворимость в воде: Многие кислоты хорошо растворяются в воде.
- Водородные ионы: Основные кислоты обладают способностью выделять водородные ионы в растворе.
- Коррозия: Многие кислоты обладают способностью разрушать металлы при контакте.
Применение основных кислот:
Основные кислоты имеют широкий спектр применения в различных отраслях жизни и промышленности, включая:
- Пищевую и напитковую промышленность: кислоты используются как консерванты, регуляторы кислотности и антиоксиданты.
- Производство удобрений: минеральные кислоты используются для получения удобрений.
- Производство лекарств: органические кислоты используются в качестве активных компонентов в лекарственных препаратах.
- Химическая промышленность: кислоты используются для синтеза органических соединений, производства пластмасс и других химических продуктов.
- Электроэнергетика: кислоты используются для обслуживания аккумуляторов и автомобильных батарей.
Примеры основных кислот:
| Тип кислоты | Примеры |
|---|---|
| Минеральные кислоты | Серная кислота (H2SO4), соляная кислота (HCl), азотная кислота (HNO3) |
| Органические кислоты | Уксусная кислота (CH3COOH), лимонная кислота (C6H8O7), яблочная кислота (C4H6O5) |





