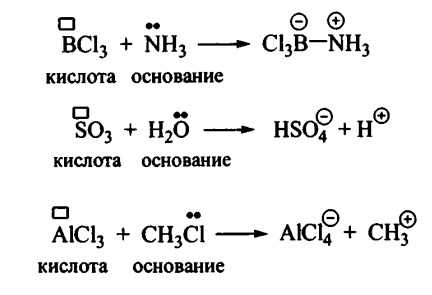
Когда мы говорим о химии, одним из важных понятий являются кислоты. Кислоты — это соединения, которые обладают способностью отдавать протоны и образовывать положительные ионы. Они имеют свойства, которые делают их уникальными и полезными в различных областях науки и промышленности.
Основные свойства кислот включают кислотность, реакцию с основаниями, изменение окраски индикаторов и электролитическую проводимость. Примерами основных кислот являются соляная кислота, серная и уксусная кислоты. Изучение этих кислот и их свойств помогает нам лучше понять химические процессы, происходящие в нашей окружающей среде.
Основное понятие кислот
Кислоты обладают несколькими общими свойствами, которые позволяют их отличать от других веществ. Одной из ключевых характеристик является их кислотность. Она проявляется в том, что кислоты способны отдавать свободные положительные ионы в растворе. Также кислоты имеют сильную афинитетность к воде, что позволяет им легко растворяться в водных средах.
Существует много различных типов кислот, от минеральных до органических. Минеральные кислоты обычно производятся из неорганических соединений. Это включает в себя такие кислоты, как серная, соляная и азотная кислоты. Органические кислоты, напротив, производятся из органических соединений и включают в себя такие кислоты, как уксусная и яблочная.
Кислоты находят широкое применение в различных областях. Например, соляная кислота часто используется в процессах очистки и обработки металлов, а уксусная кислота — в качестве пищевой добавки или консерванта. Кислоты также могут быть использованы в лаборатории для проведения различных химических экспериментов.
Чтобы более полно понять и оценить различные типы кислот, важно изучить их свойства и связанные с ними реакции. Например, когда кислоты реагируют с основаниями, они образуют соль и воду, что называется нейтрализационной реакцией. Это одно из основных свойств кислот, которое определяет их влияние на окружающую среду.
Таким образом, понимание основного понятия кислот позволяет нам использовать их в наших повседневных задачах и более глубоко исследовать их химические свойства и реакции. Кислоты играют важную роль в нашей жизни и являются неотъемлемой частью нашего окружающего мира.
Свойства кислот
Кислотность
Одно из основных свойств кислот – кислотность. Когда кислота растворяется в воде, она образует ион водорода (H+). Именно наличие этих ионов и делает кислоты кислыми. Кислотность измеряется с помощью pH-шкалы, которая варьируется от 0 до 14. Если раствор имеет pH ниже 7, он считается кислотным.
Коррозия

Кислоты известны своей способностью вызывать коррозию различных материалов, таких как металлы. При взаимодействии с кислотой, металл может окисляться и разрушаться, что приводит к коррозии и изменению свойств материала. Коррозия может быть опасной, так как она может привести к повреждению механизмов и структур, включая инфраструктуру и технологическое оборудование.
Отдавание протона
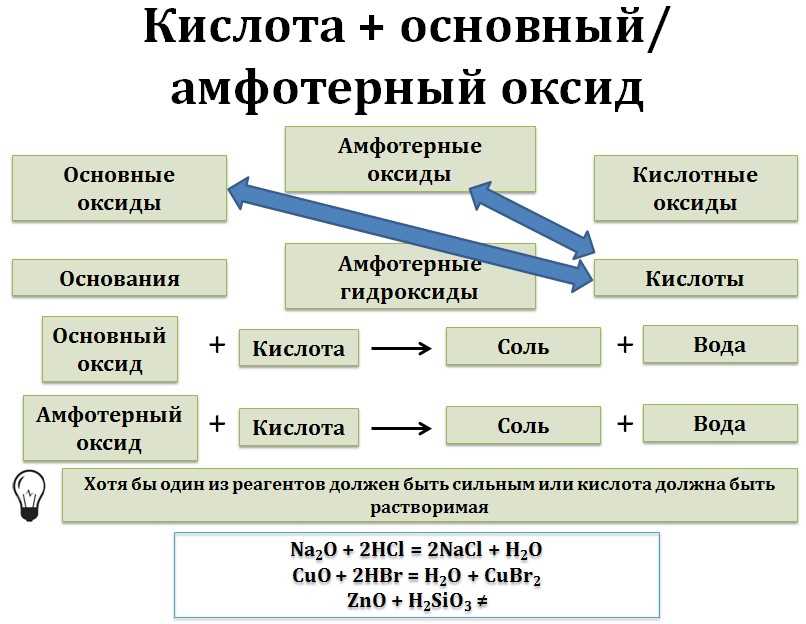
Кислоты имеют способность отдавать протоны (H+) или водородные ионы другим веществам. Это позволяет им реагировать с основаниями и образовывать соли и воду. Процесс отдавания протона называется протонированием. Например, когда кислота реагирует с гидроксидом натрия, образуется соль натрия и вода.
Коррозия металлов
Кислоты могут вызывать коррозию металлов, особенно активных металлов, таких как алюминий и железо. Когда кислота взаимодействует с металлом, происходит химическая реакция, которая разрушает металлическую структуру и вызывает образование окиси металла. Это может привести к повреждению или разрушению изделий, содержащих металлические компоненты.
Степень диссоциации
Степень диссоциации – это мера, которая определяет, насколько хорошо кислота расщепляется на ионы в растворе. Кислоты могут иметь разные степени диссоциации в зависимости от их химического состава и концентрации. Высокая степень диссоциации обеспечивает сильную кислотность и способствует быстрой реакции с другими веществами.
Примеры кислот
В природе существует множество различных кислот, каждая из которых обладает уникальными свойствами и применением. Некоторые из наиболее распространенных кислот включают соляную кислоту, азотную кислоту, серную кислоту и уксусную кислоту.
Основные кислоты в химии: понятие, свойства и примеры
Основные свойства кислот:
- Кислотные растворы имеют низкий pH. pH кислотного раствора обычно меньше 7. Количество водородных ионов (H+) в кислотном растворе больше, чем гидроксидных ионов (OH-).
- Кислоты обладают едким вкусом и способны вызывать раздражение на коже и слизистых оболочках. Их употребление в больших количествах может быть опасно для здоровья.
- Они обычно реагируют с металлами, образуя соли и выделяя водород. Некоторые кислоты, такие как соляная кислота (HCl) и серная кислота (H2SO4), могут быть очень агрессивными и опасными для работы с ними.
Некоторые примеры основных кислот:
- Соляная кислота (HCl). Она является одной из самых распространенных кислот и широко используется в промышленности, лабораториях и быту. Например, она используется для очистки металлических поверхностей, регулирования pH в бассейнах и для производства удобрений и пластмасс.
- Серная кислота (H2SO4). Она является одной из наиболее сильных кислот и также широко используется в промышленности. Она применяется в процессе производства удобрений, в производстве автомобилей и в батареях для аккумуляторов.
- Азотная кислота (HNO3). Она также является сильной кислотой и используется в промышленности для производства удобрений, пластмасс и взрывчатых веществ.
- Уксусная кислота (CH3COOH). Эта кислота часто используется в быту, особенно в кулинарии. Она содержится в уксусе и служит для консервации, маринования и добавления вкуса к пище.
Основные кислоты играют важную роль в химии и имеют множество применений в различных отраслях промышленности и в нашей повседневной жизни.