Когда мы говорим о химии, мы часто сталкиваемся с различными научными терминами, которые определяют основные концепции и понятия в этой области. Понимание этих терминов и их значения играет важную роль в изучении и использовании химии в повседневной жизни. В этой статье мы рассмотрим некоторые из основных научных терминов в химии и их значения, чтобы помочь нам более полно понять и оценить мир вокруг нас.
Атом

Атомы имеют свойства кимической индивидуальности, то есть различаются по своим химическим свойствам. Например, атомы кислорода обладают отрицательным зарядом и легко соединяются с другими атомами для образования молекул. Атомы железа, напротив, имеют положительную заряд и образуют соединения с атомами кислорода для образования оксидов.
Благодаря своей уникальной структуре и свойствам, атомы образуют различные вещества и соединения, которые мы видим вокруг себя. Например, вода состоит из атомов кислорода и водорода, а сахар состоит из атомов углерода, водорода и кислорода. Именно комбинация различных атомов, их связей и взаимодействий дает нам удивительное разнообразие веществ и материалов, которые мы используем в нашей повседневной жизни.
Понимание структуры атома и его свойств является основой для понимания химии и многих других научных дисциплин. Знание о том, как атомы взаимодействуют друг с другом, позволяет нам объяснить и предсказать реакции и превращения веществ, что имеет огромное практическое значение.
Интересно, что современные научные исследования позволили не только непосредственно наблюдать атомы, но и контролировать их свойства. Ученые смогли создать искусственные атомы и модифицировать их, что открывает новые перспективы в различных областях, включая энергетику, медицину и информационные технологии.
Так что следующий раз, когда вы задумываетесь о своем мире и окружающей вас материи, помните, что все начинается с маленьких, но невероятно важных атомов, о которых мы узнали в химии. Какие еще вопросы у вас возникают о структуре и свойствах атомов? Что вам интересно знать о химии и научных понятиях в этой области?
Элемент
В химии элемент определяется как вещество, состоящее только из одного типа атомов. Если вы оглянетесь вокруг, то увидите множество различных веществ, и многие из них представлены в таблице Менделеева — списка элементов, в котором они упорядочены по возрастающей атомной массе. Поэтому можно сказать, что элементы являются строительными блоками химического мира.
Очень удобно, что элементы имеют свои уникальные символы, такие как H (водород), O (кислород), C (углерод) и т.д. Это позволяет нам легко идентифицировать элементы и использовать их в химических формулах и уравнениях. Например, вода — это соединение из двух атомов водорода (H) и одного атома кислорода (O), поэтому мы обозначаем его формулой H₂O.
Как вы думаете, сколько элементов известно человечеству? Если сказать, что их больше 100, вы были бы правы. На данный момент в таблице Менделеева представлено 118 элементов, и каждый из них имеет свои уникальные свойства и химические реакции. Каждый элемент имеет свое местоположение в таблице Менделеева, которое определяет его химические свойства и химическую активность. Атомы элементов объединяются друг с другом, чтобы образовывать химические соединения, которые обладают различными свойствами и применениями.
И вот здесь возникает интересный вопрос: а что будет, если мы найдем новый элемент? Что, если родится новое соединение или материал, способный изменить мир? Для этого существуют ученые и исследователи, которые постоянно ищут и открывают новые элементы. Такие открытия не только расширяют наши знания о мире, но и могут привести к разработке новых материалов и технологий, которые могут улучшить нашу жизнь.
Итак, элементы представляют собой фундаментальные строительные блоки всего материального мира. Они имеют уникальные свойства и символы, которые позволяют нам идентифицировать и использовать их в различных химических процессах. Открытие новых элементов может привести к новым открытиям и технологиям, что делает химию удивительно интересной наукой.
Соединение
Представьте себе наш мир без соединений. Было бы невозможно использовать автомобиль или телефон, потому что они бы не работали без электрических соединений. Мы бы не могли иметь доступ к питьевой воде без водопроводных соединений. Даже ваши джинсы — это соединение различных волокон, которые создают прочную ткань.
Соединения могут быть органическими или неорганическими. Органические соединения содержат углерод и играют важную роль в живой природе. Они являются основой для всех жизненно важных органических молекул, таких как ДНК, протеины, жиры и углеводы.
Неорганические соединения включают в себя множество других веществ, таких как соли, оксиды, кислоты и основания. Они используются в промышленности, медицине, сельском хозяйстве и других областях науки и технологий.
Соединения могут иметь различные физические и химические свойства, которые определяют их их использование и влияние на окружающую среду. Некоторые соединения являются токсичными и опасными для здоровья человека и окружающей среды, в то время как другие могут быть полезными и важными для нашего здоровья и благополучия.
История развития химии от древних времен до наших дней неразрывно связана со сведениями о химических соединениях. Широкое использование соединений и открытие новых соединений стала возможной благодаря развитию методов анализа и синтеза в химической науке.
Так что, следующий раз, когда вы встретите слово «соединение», подумайте о широком мире химии, который оно представляет. От построения мостов до создания лекарств, соединения играют важную роль в нашей жизни и обеспечивают гораздо больше, чем мы можем себе представить.
Молекула
Когда ты слышишь слово «молекула», что в первую очередь приходит на ум? Может быть, это картинка микроскопических частиц, которые образуют твердые вещества, жидкости или газы. И ты был бы прав! Молекулы находятся везде вокруг нас – в воздухе, воде, пище, даже в нас самих! Наш мир состоит из огромного количества различных молекул, каждая из которых имеет свою уникальную структуру и функцию.
Молекулы состоят из атомов, которые соединены между собой химическими связями. К примеру, вода – это молекула, состоящая из двух атомов водорода и одного атома кислорода, которые соединены между собой. Такие соединения атомов образуют различные вещества, которые мы называем химическими соединениями.
Важно отметить, что каждый вид химического вещества имеет свою характерную структуру молекулы. Некоторые молекулы могут быть простыми и состоять всего из нескольких атомов, в то время как другие молекулы могут быть очень сложными, состоять из множества атомов и иметь сложную трехмерную структуру.
Молекулы играют ключевую роль в химических реакциях и процессах, происходящих в нашей жизни. Они определяют физические и химические свойства вещества, влияют на его состояние и реактивность. К примеру, благодаря структуре и взаимодействию молекул, мы можем наслаждаться запахом цветов или вкусом еды, работать с различными материалами, получать энергию из пищи, даже дышать и двигаться.
Так что, давайте перестанем узнавать о химии только в школе и начнем применять наши знания в повседневной жизни! Разберемся в строении и взаимодействии молекул, чтобы лучше понять, как работает наш мир и как мы можем влиять на него.
Массовое число
Давайте поговорим о таком понятии в химии, как массовое число. Ты, наверное, знаешь, что в атоме есть протоны и нейтроны, правда? Именно массовое число нам говорит о количестве этих частиц.
Так вот, массовое число — это сумма протонов и нейтронов в атоме. И знаешь что интересно? Чем больше массовое число, тем тяжелее элемент. Это логично, ведь проtons и нейтроны имеют массу, а значит, чем их больше, тем больше будет весит атом.
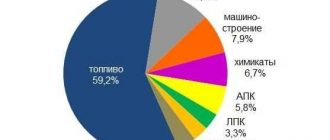
А тебе интересно знать примеры элементов с большим массовым числом? Вот их список! Самый тяжелый из них — уран с массовым числом 92. А после него идут плутоний (94), нептуний (93) и топливо, которое мы используем для ядерной энергии — плутоний (94). Все они очень тяжелые и окрашены вразные цвета! Невероятно, правда?
Массовое число очень важно для понимания элементов и их свойств. Оно помогает определить, насколько тяжелый атом и какие реакции он может претерпеть. Без массового числа, было бы очень трудно изучать и понимать мир атомов и элементов.
А сейчас, попробуй ответить на вопрос: какая разница между атомами, у которых разное массовое число?
Я надеюсь, что ты лучше познал мир атомов и элементов! Продолжай быть любознательным и искать новые знания. Ведь мир химии, такой разнообразный и увлекательный, ждет тебя!
Научные понятия в химии: основные термины и их значение
1. Вещество
Вещество — это материальная субстанция, обладающая массой и объемом. Вещество может существовать в трех состояниях: твердом, жидком и газообразном. Каждое вещество имеет свои уникальные свойства, такие как температура плавления и кипения, плотность, растворимость и т.д.
2. Элемент
Элемент — это чистое вещество, состоящее из атомов одного типа. В таблице химических элементов Менделеева представлено 118 элементов, каждый из которых имеет свой уникальный символ. Примеры элементов: кислород (O), углерод (C), железо (Fe).
3. Соединение

Соединение — это химическое вещество, образованное соединением атомов различных элементов в определенной пропорции. Соединения имеют свои химические формулы, которые указывают на количество и тип атомов, входящих в состав соединения. Примеры соединений: вода (H2O), аммиак (NH3), соль (NaCl).
4. Атом
Атом — это наименьшая единица химического элемента, которая сохраняет его химические свойства. Атомы состоят из ядра, в котором находятся протоны и нейтроны, и облака электронов, вращающихся вокруг ядра. Различные элементы отличаются по числу протонов в ядре.
5. Реакция
Химическая реакция — это превращение одних веществ (реагентов) в другие (продукты) под воздействием различных факторов, таких как температура, давление, растворители и катализаторы. Во время химической реакции происходят разрывы и образования химических связей между атомами.
6. Молекула
Молекула — это наименьшая частица соединения, которая сохраняет его химические свойства. Молекулы состоят из атомов, связанных между собой химическими связями. Различные соединения имеют разное количество и тип атомов в молекуле.
7. Химическая связь
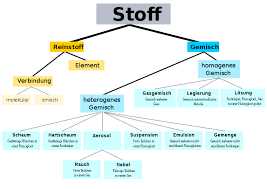
Химическая связь — это сила, удерживающая атомы в молекулах и ионах. Химические связи могут быть ковалентными, ионными или металлическими и определяют химические и физические свойства вещества. Ковалентная связь образуется при обмене электронами между атомами, ионная связь образуется при передаче электронов от одного атома другому, а металлическая связь характерна для металлов.
8. Изомерия
Изомерия — это явление, при котором две или более соединений имеют одинаковый химический состав, но различаются по своей структуре или пространственному расположению атомов. Изомеры могут иметь разные физические и химические свойства.
9. Катализатор
Катализатор — это вещество, которое ускоряет химическую реакцию, не участвуя в ней. Катализаторы снижают активационную энергию реакции, что позволяет процессу протекать быстрее. Катализаторы могут быть гомогенными, когда они находятся в одной фазе с реагентами, или гетерогенными, когда они находятся в другой фазе.
10. Молярная масса
Молярная масса — это масса одного моля вещества, выраженная в граммах. Молярная масса вычисляется путем суммирования атомных масс всех атомов в молекуле. Единица измерения молярной массы — грам/моль.