Вода – одно из самых уникальных веществ на Земле. Мы все знаем, что вода замерзает при температуре 0°C при нормальном давлении. Но что происходит с водой, когда на нее действует давление?
Оказывается, при увеличении давления точка замерзания воды смещается вниз по шкале температуры. Это означает, что при повышенном давлении вода может оставаться жидкой при очень низких температурах. Например, под давлением около 1000 атмосфер вода может не замерзнуть даже при температуре -22°C! Такое поведение называется аномальной кристаллизацией воды.
Ученые все еще исследуют и пытаются понять все тайны этого необычного явления. Пока остается много неизвестных факторов, но изучение аномальной кристаллизации воды имеет большое значение для понимания различных процессов, как естественных, так и промышленных.
Вода — особенное вещество
Не только она обеспечивает нам жизнь, но и имеет некоторые уникальные физические свойства. Например, вода является единственным веществом, которое может существовать в трех состояниях: твердом, жидком и газообразном. Размышлял ли ты когда-нибудь о том, почему лед плавается в воде? Это из-за плотности вещества! Когда вода замерзает, она расширяется и становится менее плотной, чем в жидком состоянии.
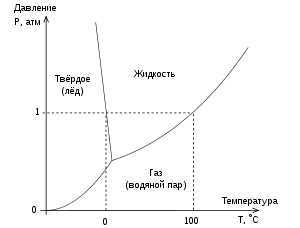
Еще одна интересная вещь о воде — ее точка замерзания. Вода обычно замерзает при 0 градусах по Цельсию, но если поднять давление, то точка замерзания может снизиться. В зависимости от величины давления, вода может оставаться в жидком состоянии даже при отрицательных температурах.
Вода имеет еще множество других удивительных свойств и особенностей. Например, она отлично проводит электричество благодаря наличию ионов. Также, вода может быть сильным растворителем, способным растворять множество веществ. Это помогает нам в чистке, готовке и множестве других процессах.
Так что следует запомнить: вода — наше богатство, и она обладает удивительными свойствами! Насколько Ты находишь воду удивительной?
Структура воды
Структура воды основывается на молекулярном уровне. Молекула воды состоит из двух атомов водорода и одного атома кислорода, связанных с помощью ковалентных связей. Эти связи образуют форму угла, известную как угол воды, который составляет около 104,5 градусов.
Уникальная структура воды заключается в ее способности образовывать водородные связи. Молекулы воды могут притягивать друг друга благодаря водородным связям между атомами водорода одной молекулы и атомом кислорода другой молекулы. Это приводит к образованию кластеров, которые держат молекулы воды вместе и создают свойства воды, такие как ее высокая плотность и поверхностное натяжение.
Кроме того, вода обладает способностью образовывать кристаллическую сетку при замерзании. При низких температурах молекулы воды начинают упорядочиваться и формировать шестиугольные решетки, что приводит к образованию льда.
Интересно, что именно эта способность образовывать кристаллическую сетку делает лед менее плотным, чем жидкая вода, поэтому лед плавает на поверхности озер и рек, предохраняя жизнь в водных экосистемах.
Свойства воды
Вода обладает так называемыми термическими свойствами. Она имеет высокую теплоемкость, что означает, что для нагревания воды требуется много энергии. За счет этого свойства вода способна сохранять стабильную температуру, что очень важно для поддержания жизни на Земле.
Кроме того, вода обладает высокой теплопроводностью, что означает, что она быстро распространяет тепло. Это делает ее полезной в различных инженерных системах и технологических процессах.
Еще одним интересным свойством воды является ее аномальное тепловое расширение. Когда вода замерзает, она расширяется, а не сжимается, как большинство других веществ. Это объясняет, почему лед на поверхности воды плавает. Если бы лед был более плотным, то вся вода в озерах и реках замерзала бы, предотвращая жизнь в них.
Еще одним важным свойством воды является ее способность растворять многие вещества. Вода — универсальный растворитель, и благодаря этому мы можем получать много полезных веществ из природы.
Кроме того, вода обладает поверхностным натяжением, что позволяет ей образовывать капли и пузырьки. Это свойство играет важную роль в живых организмах, так как позволяет им передвигаться через воду или даже на ней.
Наконец, вода является отличным растворителем для многих веществ. Благодаря этому свойству она способствует химическим реакциям в нашем организме и помогает нам питаться и дышать.
Вода — это драгоценный ресурс, который нам необходим для жизни. Мы должны бережно относиться к нему и стремиться сохранить его чистоту и доступность для всех. Каждый из нас может внести свой вклад в сохранение и защиту воды. Будьте осторожны с ее использованием, соблюдайте экологические правила и образ жизни, чтобы наслаждаться всеми прекрасными свойствами этого волшебного вещества.
Вода под давлением
Когда давление увеличивается, точка замерзания воды также повышается. Например, при давлении 10 MPa (мегапаскаль), точка замерзания воды может быть около -5°C. Это объясняется тем, что при давлении между молекулами воды образуются связи, которые затрудняют движение и образование кристаллов льда.
С другой стороны, если давление снижается, точка замерзания воды снижается. Например, на высоких горных вершинах, где атмосферное давление ниже, вода может замерзать при температуре ниже 0°C. Это может быть причиной образования ледников и снега на высоте, где обычно жидкая вода не замерзает.
Таким образом, вода под давлением может замерзать при разных температурах в зависимости от изменения давления. Это интересное явление, которое можно увидеть в различных условиях, от экспериментов в лаборатории до природных процессов на Земле.
Влияние давления на свойства воды
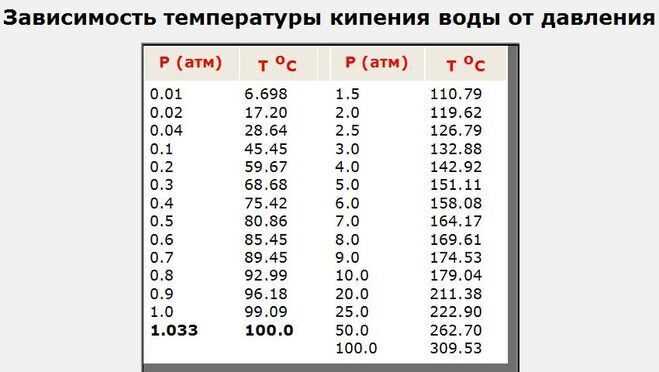
В школе, вы, вероятно, узнали, что вода замерзает при температуре 0 градусов Цельсия. Но что происходит с водой, когда она находится под давлением? На самом деле, под воздействием давления температура замерзания воды может изменяться.
Когда давление повышается, точка замерзания воды снижается. Это происходит из-за того, что давление подавляет кинетическую энергию молекул воды, что затрудняет их перемещение и образование кристаллов льда. Таким образом, под высоким давлением вода может оставаться в жидком состоянии при температурах ниже нуля градусов Цельсия.
Например, вода в озере Байкал, который находится под давлением в результате глубокого расположения, может оставаться жидкой даже при очень низких температурах, так как давление помогает подавить фазовый переход от жидкости к льду.
Это интересное свойство воды может иметь важные практические применения. Например, в науке и технологии, подавленная точка замерзания воды может использоваться в процессе криогенной консервации, холодильной технике и даже в производстве пищевых продуктов.
Таким образом, давление оказывает значительное влияние на свойства воды, включая ее температуру замерзания. Это уникальное свойство позволяет воде оставаться в жидком состоянии даже при низких температурах и может быть использовано в различных отраслях промышленности и науки.
Температура замерзания под давлением
Но, оказывается, вода — уникальное вещество. Когда на нее действует давление, ее точка замерзания снижается. Это происходит из-за того, что давление позволяет молекулам воды быть плотнее, и они труднее образуют лед.
Знаешь, интересный факт: при давлении около 2,000 атмосфер (что эквивалентно глубине около 6,000 метров), вода может оставаться жидкой при температуре, ниже нуля градусов Цельсия! Это называется «сверхохлаждение». Но, стоит внести хоть малейшую колеблющуюся частицу, и она моментально замерзнет.
Кстати, здесь есть еще одна интересная вещь: вода может замерзать при меньшей температуре, если в ней есть примеси. Например, если в воде есть соль или специальные химические соединения, то она будет замерзать уже при отрицательной температуре.
А ты знал об этом? Как думаешь, почему вода замерзает под давлением? Пиши в комментариях!
Закон замерзания под давлением
Когда на улице холодно, мы знаем, что вода может замерзать и превращаться в лед. Но что происходит с водой при давлении? И как это связано с законом замерзания под давлением?
Начнем с основного: вода замерзает, когда ее температура достигает определенного уровня, который зависит от давления. Под давлением, вода может оставаться жидкой при температурах ниже обычной точки замерзания. Это происходит потому, что давление сдерживает образование ледяных кристаллов.
Закон замерзания под давлением гласит, что с повышением давления точка замерзания также повышается. Когда вода находится под высоким давлением, она может оставаться жидкой при нижних температурах.
Этот закон имеет широкое практическое применение. Например, он используется в технике, чтобы предотвратить замерзание воды в трубах при низких температурах. Применение давления позволяет сохранить воду в жидком состоянии, даже если температура опускается ниже обычной точки замерзания.
Если ты когда-нибудь сталкиваешься с проблемой замерзания воды в морозную погоду, теперь ты знаешь, как применить закон замерзания под давлением, чтобы предотвратить этот неприятный инцидент. Просто увеличь давление или используй теплоизоляционные материалы, чтобы сохранить воду в жидком состоянии.
Описание закона замерзания под давлением
Ты когда-нибудь задумывался, почему вода замерзает при определенной температуре? А особенно интересно, что происходит, когда вода замерзает под давлением?
Так вот, существует закон замерзания под давлением. По этому закону, при увеличении давления на жидкость, ее температура замерзания снижается. Это означает, что вода может оставаться жидкой при температурах ниже нуля градусов Цельсия, если на нее действует достаточно большое давление.
Но что происходит, когда вода замерзает под давлением? Кристаллы льда, образующиеся при замерзании, занимают больше места, чем вода в жидком состоянии. Под давлением, молекулы воды сжимаются, и это позволяет им сохранять жидкое состояние при более низкой температуре, чем без давления.
Такой закон замерзания под давлением играет важную роль в природе. Например, подо льдом на озере или реке вода может оставаться жидкой, потому что давление от льда сдерживает замерзание. Это позволяет рыбам и другим организмам выживать в холодных условиях.
Так что, вот тебе небольшая интересная информация о законе замерзания под давлением. И да, следующий раз, когда вода замерзнет, ты уже знаешь, почему это происходит!
Применение закона в научных и промышленных целях
Закон о температуре замерзания воды под давлением имеет множество научных и промышленных применений. Он играет ключевую роль в различных областях, от химической промышленности до геологии.
В химической промышленности точное знание о температуре замерзания воды под давлением позволяет управлять процессами замораживания и кристаллизации различных веществ. Это особенно важно при производстве лекарственных препаратов, пищевых продуктов и химических соединений. Знание точной температуры замерзания воды позволяет улучшить качество и стабильность продуктов, а также оптимизировать процессы производства.
В геологии закон о температуре замерзания воды под давлением используется для изучения ледниковых периодов и климатических изменений. Путем анализа температурных показателей можно определить историю погоды и климата в разных районах Земли. Это информация критически важна при изучении изменений климата и их влияния на окружающую среду.
Кроме того, понимание закона о температуре замерзания воды под давлением имеет практическое применение в различных инженерных системах, таких как отопление и холодильные установки. Знание точной температуры замерзания воды позволяет эффективно контролировать работу систем и избежать проблем, связанных с замерзанием или перегревом жидкости.
Применение закона о температуре замерзания воды под давлением помогает улучшить наши жизни и окружающую среду. Благодаря этому закону мы можем создавать более эффективные процессы производства, изучать климатические изменения и обеспечивать надежную работу инженерных систем. И это только небольшая часть примеров того, как научные законы могут быть применены на практике.